
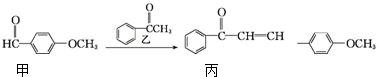
| A. | 丙的分子式为C16H14O2 | |
| B. | 丙分子中所有碳原子可能共平面 | |
| C. | 用酸性KMnO4溶液可区分甲和丙 | |
| D. | 乙在一定条件下最多与4mol氢气发生加成反应 |
分析 A.根据结构简式确定元素种类和原子个数,可确定分子式;
B.根据苯环和碳碳双键的结构特点判断;
C.甲含有醛基,丙含有碳碳双键,都可被酸性高锰酸钾氧化;
D.乙中苯环和羰基都可与氢气发生加成反应.
解答 解:A.由结构简式可知丙的分子式为C16H14O2,故A正确;
B.丙含有苯环和碳碳双键都为平面形结构,与苯环和碳碳双键直接相连的原子可能在同一个平面上,故B正确;
C.甲含有醛基,丙含有碳碳双键,都可被酸性高锰酸钾氧化,不能用高锰酸钾区分,故C错误;
D.乙中苯环和羰基都可与氢气发生加成反应,则乙在一定条件下最多与4mol氢气发生加成反应,故D正确.
故选C.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断能力,明确官能团及其性质关系是解本题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5 mol/(L•s) | B. | v(B)=0.3 mol/(L•s) | C. | v(C)=0.8 mol/(L•s) | D. | v(D)=60 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A、B、C都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式填空:
A、B、C都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式填空:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4升氧气中一定含有阿伏加德罗常数个氧分子 | |
| B. | 1摩氧气的质量是32克 | |
| C. | 1摩氧气与1摩二氧化碳中的原子个数相等 | |
| D. | H2SO4的摩尔质量是98克 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com