
| 温度/℃ | 800 | 1000 | 1100 | 1200 | 1400 |
| 平衡常数 | 0.45 | 1.92 | 48.1 | 276.5 | 1771.5 |
分析 (1)①2CO(g)+4H2 (g)?CH3CH2OH(g)+H2O(g)△H1=-a kJ•mol-1.
②H2O(l)═H2O(g)△H2=+b kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-c kJ•mol-1,
①-2×③-3×②得2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(l),依据盖斯定律计算反应热;
(2)①升高温度,平衡向吸热方向移动,吸热方向平衡常数增大;
②列三段,根据平衡常数表达式计算其数值;依据V=$\frac{△c}{△t}$计算氢气的生成速率;
(3)CH4与NO2发生反应生成无毒的N2、CO2和H2O;
(4)原电池阴离子移向负极;燃料电池中负极燃料乙醇失去电子发生氧化反应生成二氧化碳和水;
解答 解:(1)①2CO(g)+4H2 (g)?CH3CH2OH(g)+H2O(g)△H1=-a kJ•mol-1.
②H2O(l)═H2O(g)△H2=+b kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-c kJ•mol-1,
①-2×③-3×②得2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(l),依据盖斯定律该反应的反应热为:△H1-3△H2-2△H3=-(a+3b-2c)kJ•mol-1;
故答案为:-(a+3b-2c)kJ•mol-1;
(2)①依据图中数据可知,温度升高,K增大,平衡向正向移动,升高温度平衡向吸热方向移动,则正向为吸热反应;
故答案为:吸热;
②T℃时,向1L密闭容器中投入1molCH4和1mol H2O(g),平衡时c(CH4)=0.5mol•L-1,则:
CH4+H2O(g)?CO+3H2,
起始浓度:(mol/L) 1 1 0 0
转化浓度:(mol/L) $\frac{2}{3}$ $\frac{2}{3}$ $\frac{2}{3}$ 2
平衡浓度:(mol/L) $\frac{1}{3}$ $\frac{1}{3}$ $\frac{2}{3}$ 2
该温度K=$\frac{[CO]•[{H}_{2}]^{3}}{[C{H}_{4}]•[{H}_{2}O]}$=$\frac{\frac{2}{3}×{2}^{3}}{\frac{1}{3}×\frac{1}{3}}$=48mol2/L2,所以该温度为:1100;
V(H2)=$\frac{2mol/L}{5h}$=0.400mol/(L•h);
故答案为:1100℃0.400mol/(L•h);
(3)CH4与NO2发生反应生成无毒的N2、CO2和H2O,反应为CH4+2NO2 $\stackrel{催化剂}{→}$N2+CO2+2H2O.
故答案为:CH4+2NO2 $\stackrel{催化剂}{→}$N2+CO2+2H2O;
(4)原电池阴离子移向负极;通入乙醇一极是负极,该极上乙醇失去电子发生氧化反应生成二氧化碳和水,电极反应式为C2H6O+6O2--12e-=2CO2+3H2O;
故答案为:负;C2H6O+6O2--12e-=2CO2+3H2O.
点评 本题为综合题,考查了反应热的计算、化学平衡常数的计算及应用、燃料电池电极反应式的书写,题目综合性较强,难度中等.


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 胶体的分散质能透过滤纸 | B. | 胶体粒子直径在1nm~100nm之间 | ||
| C. | 胶体具有丁达尔现象 | D. | 胶体和其它分散系都是混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑥ | B. | ②④⑤⑦ | C. | 只有⑤ | D. | 均不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| 键能/kJ.mol-1 | a | b | x | c | d |
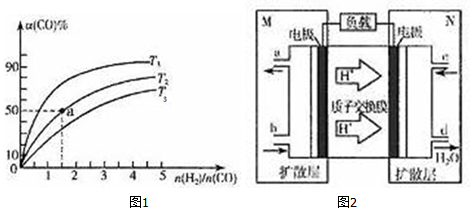
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 反应时间/min | n(CO)/mol | n (H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.20 | |
| t2 | 0.80 |
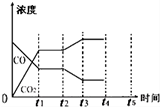
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 编号 | 热化学方程式 |
| ① | CO(g)+2H2(g)?CH3OH(g)△H1=-99kJ•mol-1 |
| ② | 2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24kJ•mol-1 |
| ③ | CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41kJ•mol-1 |
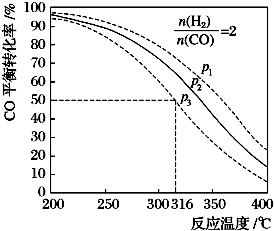
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32gO2和32gO3所含原子数目都为2NA | |
| B. | 标准状况下,11.2 L水中含有的原子数是1.5NA | |
| C. | 0.1 mol Fe参与化学反应转移的电子数一定为0.3NA | |
| D. | 在同温同压下,相同体积的任何气体单质所含的原子数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com