
【题目】有一种有机化合物,其结构简式如图,下列有关它的性质的叙述,正确的是( ) 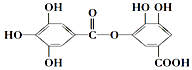
A.有弱酸性,1mol该有机物与溴水反应,最多能消耗4mol Br2
B.在一定条件下,1mol该物质最多能与7mol NaOH完全反应
C.在Ni催化下,1mol该物质可以和8mol H2发生加成反应
D.它能发生水解反应,水解后只能生成两种产物
【答案】A
【解析】解:A.酚羟基的邻、对位氢原子,可以与Br2发生取代反应,所以1 molX最多能与4 molBr2反应,故A正确; B.在1molZ中含有1mol水解后生成1mol羧基和1mol酚羟基的酯基、1mol羧基、5mol酚羟基,可以和8molNaOH发生反应,故B错误;
C.只有苯环与氢气发生加成反应,则在Ni催化下,1mol该物质可以和6mol H2发生加成反应,故C错误;
D.分子中含有酯基,能发生水解,1mol 有机物水解后能生成2mol ![]() ,故D错误.
,故D错误.
故选A.
【考点精析】认真审题,首先需要了解有机物的结构和性质(有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解).


科目:高中化学 来源: 题型:
【题目】下列除杂质(括号中物质为杂质)所用试剂或方法不正确的是( )
A.CO2(CO):O2
B.MgO(Al2O3):NaOH溶液
C.NaHCO3溶液(Na2CO3):过量的CO2
D.CO2(HCl):饱和NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将20g质量分数为14%的KNO3溶液与30g质量分数为24%的KNO3溶液混合,得到的密度为1.26 g/mL的混合溶液.计算:
(1)混合后溶液的质量分数.
(2)混合后溶液的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Sn(核电荷数为50)是人类最早使用的元素之一,能形成SnCl2 , SnCl4两种氯化物,SnCl2常温下为白色晶体,具有一维链状的聚合结构,气态时以单分子形式存在,而SnCl4常温下为无色液体.白锡和灰锡是Sn的两种同素异形体,白锡的晶体结构中Sn原子的配位数为4和6,灰锡的晶体结构与金刚石的晶体结构相似.白锡的密度大于灰锡的密度. 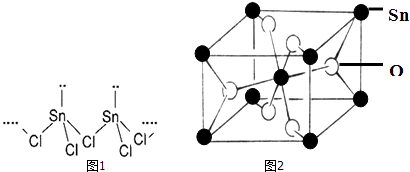
(1)Sn元素外围电子排布式为 .
(2)SnCl2的一维链状聚合结构如图1所示,在分子结构中存在的化学键是 .
(3)SnCl4与CCl4中沸点较高的是 . 原因是 .
(4)锡的某种氧化物的晶胞如图2,其化学式为 .
(5)解释白锡分子的密度大于灰锡的密度的原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 标况下,1mol任何物质的体积都约为22.4L
B. 1mol气体的体积约为22.4L
C. 标况下,1molO2和N2混合气(任意比)的体积约为22.4L
D. 22.4L气体所含分子数一定大于11.2L气体所含的分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅酸盐材料的说法错误的是
A.普通玻璃的主要成份是SiO2
B.生活中常见的硅酸盐材料有玻璃、水泥、陶瓷
C.陶瓷的主要原料是黏土
D.硅酸盐水泥以石灰石和黏土原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是 ( )
A. 12g碳所含的原子数就是阿伏加德罗常数
B. 阿伏加德罗常数没有单位
C. “物质的量”指物质的质量
D. 摩尔是表示物质的量的单位,每摩尔物质含有阿伏加德罗常数个微粒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素性质呈周期性变化的决定因素是( )
A. 元素原子半径呈周期性变化B. 元素的相对原子质量依次递增
C. 元素原子核外电子排布呈周期性变化D. 元素的最高正化合价呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氧气的反应为 2KClO3 ![]() 2KCl+3O2↑,反应后从剩余物中回收二氧化锰的操作顺序正确的是(已知MnO2为黑色难溶于水的固体)( )
2KCl+3O2↑,反应后从剩余物中回收二氧化锰的操作顺序正确的是(已知MnO2为黑色难溶于水的固体)( )
A.溶解、蒸发、洗涤、过滤
B.溶解、过滤、蒸发、洗涤
C.溶解、过滤、洗涤、干燥
D.溶解、洗涤、过滤、加热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com