
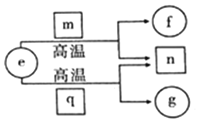
 短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )| A. | 原子半径的大小:W>Z>X | |
| B. | 简单氢化物的沸点:W>Y>Z | |
| C. | 元素Y、Z、W形成的单质不止一种 | |
| D. | 元素Y、Z、W与元素X均能形成18e-的分子 |
分析 m常温下为液态,应为H2O,短周期在高温下与水反应的单质为碳,则e为C单质,Y为C元素,由转化关系可知n为CO,f为H2,可知X为H元素,Z为O元素,固体q应为SiO2,g为Si,结合对应单质、化合物的性质以及元素周期律解答该题.
解答 解:由以上分析可知X为H、Y为C、Z为O、W为Si元素,
A.一般来说原子核外电子层数越多,原子半径越大,故A正确;
B.Z为O元素,对应氢化物分子间存在氢键,作用力较强,沸点较高,故B错误;
C.C对应的单质有金刚石、石墨等,O对应的单质有氧气、臭氧等,Si对应的单质有晶体硅、无定形硅等,故C正确;
D.元素Y、Z、W与元素X形成的化合物中C2H6、H2O2、SiH4都为18e-的分子,故D正确.
故选B.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、发生的反应、元素周期律等为解答的关键,侧重分析与推断能力的考查,注意碳与水的反应为推断的突破口,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 芳香烃都符合通式CnH2n-6(n≥6) | B. | 分子中含苯环的化合物都是芳香烃 | ||
| C. | 芳香烃都有香味,因此得名 | D. | 芳香烃属于芳香族化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(M) | n(N) | n(P) | ||
| ① | 500 | 0.3 | 0.2 | 0.3 |
| ② | 600 | 0.2 | 0.3 | 0.24 |
| ③ | 750 | 0.1 | 0.1 | x |
| A. | 实验①中,若5 min时测得n(N)=0.050 mol,则0~5min时间内平均反应速率v(P)=0.015 mo1/(L•min) | |
| B. | 实验②中达到平衡后,增大压强,M的转化率增大,平衡常数不变 | |
| C. | 600℃时该反应的平衡常数K=3.0 | |
| D. | 实验③中,达到平衡时,x<0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C、D、E的简单离子半径由大到小的顺序是E>D>C | |
| B. | 含有E的盐溶液可能显酸性、可能显中性、也可能显碱性 | |
| C. | A和C形成的化合物中一定只有极性键 | |
| D. | BC2跟C、E形成的化合物发生的反应都是非氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 298 K时,加蒸馏水稀释HF溶液,$\frac{c({F}^{-})}{c(HF)}$保持不变 | |
| B. | 308 K时,HF的电离常数Ka>3.5×10-4 | |
| C. | 298 K时,向饱和CaF2溶液中加入少量CaCl2,Ksp(CaF2)会减小 | |
| D. | 2HF(aq)+Ca2+(aq)?CaF2(s)+2H+(aq) K≈0.68 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鉴别己烷、己烯和乙醇,可用溴水 | |
| B. | 乙烯和植物油均能使溴的四氯化碳溶液褪色,且反应原理相同 | |
| C. | 甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种 | |
| D. | 1mol分子式为C18H26O5的酯完全水解生成lmol 羧酸和2mol乙醇,该羧酸分子式为C14H18O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
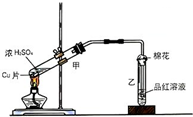 如图为浓硫酸与铜片反应的装置.请回答:
如图为浓硫酸与铜片反应的装置.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:1 | C. | 2:5 | D. | 5:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com