
下列关于金属冶炼的说法正确的是
A.金属冶炼的本质是将化合态金属还原为游离态,冶炼方法由金属的活泼性决定
B.Cu的湿法冶炼是将金属钠投入到CuSO4溶液中,从而置换出铜
C.Fe通常采用热还原法冶炼,加入石灰石的目的是除去过量的碳
D.由于Al的活泼性强,故工业上采用电解熔融AlCl3的方法生产Al
A
【解析】
试题分析:金属的冶炼有三种方法,依据金属活动顺序在K-Al采用电解法,Zn-Cu采用热还原法,Hg以后采用热分解法。故A正确;B选项,钠与CuSO4溶液反应首先Na与H2O反应,然后生成的NaOH再与CuSO4反应无法置换Cu,故B错误;C选项,石灰石中的碳酸钙在高温条件下分解能生成氧化钙和二氧化碳,氧化钙能和二氧化硅反应生成硅酸钙,从而除去铁矿石中的二氧化硅,即炼铁高炉中加入石灰石的目的是除去脉石(二氧化硅),故C错误;D选项,由于AlCl3是共价化合物,故不能用电解熔融AlCl3的方法生产Al,应该用2Al2O3(熔融) 4Al+3O2↑,故D错误。
4Al+3O2↑,故D错误。
考点:金属的冶炼 金属活动顺序
点评:本题难度适中,但是错误选项的迷惑性很大,同学们背诵了金属活动顺序,受到思维定势影响,忽视了Na先与水反应的事实,而铁的冶炼,加入石灰石是利用氧化钙除去二氧化硅对学生来讲比较陌生,Al的冶炼,同学们对典型的金属与非金属形成了共价化合物AlCl3理解起来困难。


科目:高中化学 来源:2014-2015学年陕西省安康市高三上学期第二次教学质量调研化学试卷(解析版) 题型:选择题
700℃时,向容积不变的1L密闭容器中充人一定量的CO和H2O,发生反应:
CO(g)+ H2O(g) CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t1<t2)
CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t1<t2)

下列说法不正确的是
A.O-t1 min的平均反应速率为v(H2)=  mol·L-l.min-1
mol·L-l.min-1
B.保持其他条件不变,若容器内的压强不改变时,该反应一定达到了化学平衡状态
C.保持其他条件不变,若起始时向容器中充入0.60mol CO和1.20mol H2O,则达到平衡时n(CO2)=0.40mol
D.保持其他条件不变,向平衡体系中再通入0.20mol H2O,与原平衡相比,达到新平衡时CO的转化率增大,CO2的浓度增大
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省盐城市高二12月月考化学试卷(解析版) 题型:选择题
14.重水D2O的离子积为1.6×10-15,可以用PH一样的定义来规定PD= —lgc(D+),以下关于PD的叙述正确的是
A.中性溶液中PD=7
B.在1LD2O的溶液中溶解0.01mol NaOD(设溶液的体积为1L),其中PD=12
C.在1L D2O中溶解 0.01mol DCl(设溶液的体积为1L),其中PD=2
D.在100mL 0.25mol·L-1的NaOD重水溶液中加入50mL 0.2mol·L-1DCl的的重水溶液,其中PD=1
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:填空题
(19分)某化学课外兴趣小组为探究铜与浓硫酸的反应,用下图所示的装置进行实验:


请回答下列问题:
(1)B是用收集实验中产生气体的装置,但未将导管画全,请将装置图补充完整。
(2)实验中他们取6.4g铜片和12mL18mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余。
①写出铜与浓硫酸反应的化学方程式:_________________________________________;
实验中若有m g铜参加了反应,则有______mol硫酸被还原,电子转移数目为___。
②下列试剂中,能证明反应停止后烧瓶中有硫酸剩余的是__________(填写字母编号)。
A.硫酸钠溶液 B.氯化钡溶液 C.银粉 D.碳酸钠溶液
③为什么有一定量的硫酸剩余但未能使铜片完全溶解?你认为的原因是
__________________________________________________________________。
(3)为了测定消耗硫酸的物质的量,该兴趣小组设计了两个实验方案:
方案一:将装置A产生的气体缓缓通过已称量过的装有碱石灰的干燥管,反应停止后再次称量,两次质量差即是吸收的二氧化硫。
方案二:将装置A产生的气体缓缓通入足量的用硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称得沉淀的质量即是二氧化硫转化为硫酸钡沉淀的质量。
实际上,方案一、二均不可取。
方案一产生的气体中含有 ,使干燥管增重偏大;也可能由于
,使干燥管增重偏小。
方案二:由于 与氯化钡溶液反应,使测定消耗硫酸的物质的量结果偏大。
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
下列各反应中,划线的反应物能够完全消耗的是
A.溶于水的氯气 B.足量的一氧化碳与氧化铝
C.足量的MnO2与浓盐酸共热 D.足量的铁与浓硫酸共热
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
下列物质的俗称、主要成分的化学式及其用途均正确的是
A.磁铁矿——Fe2O3——炼铁 B.胆矾——CuSO4·5H2O——波尔多液
C.蓝宝石——SiO2——饰品 D.纯碱——NaHCO3——焙制糕点
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三“一诊”理综化学试卷(解析版) 题型:填空题
(14分)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2 H2(g)+CO(g) CH3OH(g);
CH3OH(g);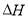 =-a KJ·mol-1(a>0)。初始投料与各容器达到平衡时的有关数据如下:
=-a KJ·mol-1(a>0)。初始投料与各容器达到平衡时的有关数据如下:
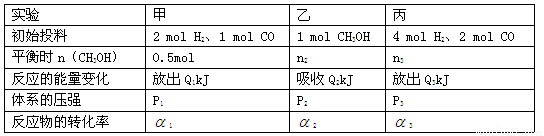
(1)该温度下此反应反应物的总键能和 (填“大于”“等于”或“小于”)生成物的总键能和。
(2)在该温度下,假设甲容器从反应开始到平衡所需时间为4 min,则H2的平均反应速率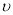 ( H2)为 。
( H2)为 。
(3)下列选项能说明甲容器中的反应已经达到平衡状态的有 (填序号)。
A.容器内H2、CO、CH3OH的物质的量之比为2:1:1
B.容器内气体的密度保持恒定
C.容器内H2气体的体积分数保持恒定
D.2V正(H2)=V逆(CO)
(4)丙容器中,平衡后将容器的容积压缩到原来的l/2,其他条件不变,对平衡体系产生的影响是
(填字母序号)。
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡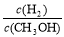 减小
减小
E.平衡常数K增大
(5)三个容器中的反应分别达平衡时各组数据关系正确的是 (填序号)。
A.Q1+Q2=a B.α3<α1
C.P3<2P1=2P2 D.n2<n3<1.0mol
(6)已知:①3CO(g) +3H2(g) CH3OCH3(g) +CO2(g) △H=—247kJ·mol-l
CH3OCH3(g) +CO2(g) △H=—247kJ·mol-l
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H= -24 kJ·mol-l
CH3OCH3(g)+H2O(g) △H= -24 kJ·mol-l
③CO(g)+H2O(g) CO2(g)+H2(g) △H= -41 kJ·mol-l
CO2(g)+H2(g) △H= -41 kJ·mol-l
2 H2(g)+CO(g) CH3OH(g);
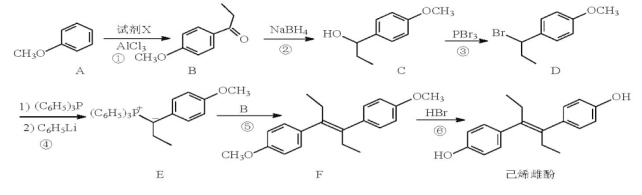
CH3OH(g);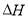 =-a KJ·mol-1 ,则 a=
=-a KJ·mol-1 ,则 a=
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都郫县高三第二次阶诊断性考试理综化学试卷(解析版) 题型:选择题
下列有关物质分类或归纳不正确的是
①电解质:明矾、冰醋酸、氯化银、纯碱 ②化合物:BaCl2、Ca(OH)2、HNO3、HT
③混合物:盐酸、漂白粉、水玻璃、水银 ④同素异形体:金刚石、石墨、C60、C70
A.①② B.②③ C.③④ D.②④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:推断题
(15分)己烯雌酚(stilbestrol)是非甾体雌激素物质,可通过以下方法合成
(1)化合物B中的含氧官能团为 和 (填名称)。
(2)反应①中加入的试剂X的分子式为C3H5ClO,X的结构简式为 。
(3)上述反应①②③⑥中,属于取代反应的是 (填序号)。
(4)B的一种同分异构体满足下列条件:
I、能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应。
II、分子中有4种不同化学环境的氢。
写出该同分异构体的结构简式: (任写一种)。
(5)根据已有知识并结合相关信息,写出以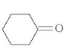 为原料制备
为原料制备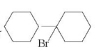 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com