
(1)将一小块金属钠投入装有硫酸铜溶液的烧杯中,现象________;化学方程式________________________.
(2)向盛有苯胺乳浊液的试管中滴入浓盐酸并振荡,现象________;化学方程式________________________.
(3)用排水法把NO收集在大试管里,将此试管倒立于水槽中,自水下向试管里通入适量氧气.现象________;化学方程式________________________.
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
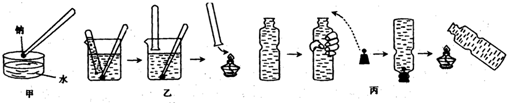
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 滴定 次数 |
待测溶液的体积 /mL |
标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 20.00 | 2.00 | 21.99 |
| 2 | 20.00 | 0.80 | 23.42 |
| 3 | 20.00 | 1.02 | 21.03 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 探究内容 | 实验方案 | 实验现象 | 写出下列离子方程式 |
| 探究Fe2+具有还原性 | 取少量0.1mol?L-1FeCl溶液,加入少量KSCN溶液后,再往溶液中加入少量 新制氯水 新制氯水 |
溶液先不变红,后变为血红色 | ①Fe2+发生的反应: 2Fe2++Cl2=2Fe3++2Cl- 2Fe2++Cl2=2Fe3++2Cl- |
| 探究Fe3+具有氧化性 | 取少量0.1mol?L-1FeCl溶液,加入足量 铁粉 铁粉 后,再往溶液中加入少量KSCN溶液 |
溶液不变为血红色 | Fe3+发生的反应: 2Fe3++Fe=3Fe2+ 2Fe3++Fe=3Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:022
完成下列实验,并描述实验现象,写出有关的化学方程式.
(1)将一小块金属钠投入装有硫酸铜溶液的烧杯中,现象________;化学方程式________________________.
(2)向盛有苯胺乳浊液的试管中滴入浓盐酸并振荡,现象________;化学方程式________________________.
(3)用排水法把NO收集在大试管里,将此试管倒立于水槽中,自水下向试管里通入适量氧气.现象________;化学方程式________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com