
”¾ĢāÄæ”æĄūÓĆĀĮ»Ņ(Ö÷ŅŖ³É·ÖĪŖAl”¢Al2O3”¢AlN”¢FeOµČ)ÖʱøĀĮ÷·¼Į”¾Ö÷ŅŖ³É·ÖĪŖAl(OH)2Cl”æµÄŅ»ÖÖ¹¤ŅÕČēĻĀ£ŗ
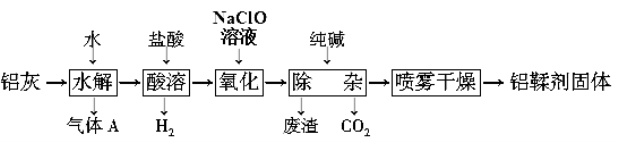
¢ÅĘųĢåAÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶”£ĀĮ»ŅŌŚ90 ”ęĖ®½āÉś³ÉAµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ ”£
¢Ę”°ĖįČÜ”±Ź±£¬Al2O3·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ ”£
¢Ē”°Ńõ»Æ”±Ź±£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ ”£
¢Č”°·ĻŌü”±³É·ÖĪŖ________(Ģī»ÆѧŹ½)”£
¢É²ÉÓĆÅēĪķøÉŌļ¶ų²»ÓĆÕō·¢µÄŌŅņŹĒ______________________”£
¢ŹģŃÉÕĮņĖįĀĮļ§¾§Ģ壬·¢ÉśµÄÖ÷ŅŖ·“Ó¦ĪŖ£ŗ
4[NH4Al(SO4)2”¤12H2O]![]() 2Al2O3+2NH3”ü+N2”ü+5SO3”ü+3SO2”ü+53H2O
2Al2O3+2NH3ӟ+N2ӟ+5SO3ӟ+3SO2ӟ+53H2O
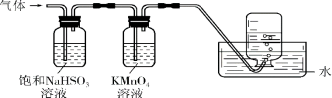
½«²śÉśµÄĘųĢåĶعżČēĻĀĶ¼ĖłŹ¾µÄ×°ÖĆ”£Ōņ¼ÆĘųĘæÖŠŹÕ¼Æµ½µÄĘųĢåŹĒ (Ģī»ÆѧŹ½)”£
”¾“š°ø”æ(1)AlN£«3H2O ![]() Al(OH)3£«NH3”ü
Al(OH)3£«NH3”ü
(2)Al2O3£«6H£«===2Al3£«£«3H2O
(3)2Fe2£«£«2H£«£«ClO£===2Fe3£«£«Cl££«H2O (4)Fe(OH)3 [
(5)·ĄÖ¹Al(OH)2ClĖ®½āÉś³ÉAl(OH)3 (6)N2
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗĀĮ»ŅÖ÷ŅŖ³É·ÖĪŖAl”¢Al2O3”¢AlN”¢FeOµČ¼ÓČėĖ®·¢Éś·“Ó¦£¬AlNŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆĀĮŗĶ°±Ęų£¬¼ÓČėŃĪĖįĖįČÜŗó£¬Éś³ÉĀČ»ÆĀĮČÜŅŗŗĶĀČ»ÆŃĒĢśČÜŅŗ£¬¼ÓČėĘÆ°×¼ĮŃõ»ÆŃĒĢśĄė×ÓĪŖĢśĄė×Ó£¬¼ÓČė“æ¼īµ÷½ŚČÜŅŗPHŹ¹ĢśĮż×ÓČ«²æ³Įµķ£¬²ÉÓĆÅēĪķøÉŌļÖʱøĀĮ÷·¼Į£»
(1)ĘųĢåAÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶£¬ĖµĆ÷Éś³ÉµÄŹĒ°±Ęų£¬ĀĮ»ŅÖŠµÄAlNŗĶĖ®·¢ÉśĖ®½ā·“Ӧɜ³ÉĒāŃõ»ÆĀĮ³ĮµķŗĶ°±Ęų£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗAlN+3H2O![]() Al(OH)3+NH3”ü£»
Al(OH)3+NH3”ü£»
(2)Ńõ»ÆĀĮŹĒĮ½ŠŌŃõ»ÆĪļĖįČÜŹ±ŗĶŃĪĖį·¢Éś·“Ӧɜ³ÉĀČ»ÆĀĮČÜŅŗ£¬)”°ĖįČÜ”±Ź±£¬Al2O3·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗAl2O3+6H+ØT2Al3++3H2O£»
(3)¼ÓČėĘÆ°×ŅŗµÄ×÷ÓĆŹĒĄūÓĆ“ĪĀČĖįøłĄė×ÓŌŚĖįČÜŅŗÖŠµÄĒæŃõ»ÆŠŌŃõ»ÆŃĒĢśĄė×ÓĪŖĢśĄė×Ó£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Fe2++2H++ClO-ØT2Fe3++Cl-+H2O£»
(4)ÉĻŹö·ÖĪöæÉÖŖ”°·ĻŌü”±³É·ÖĪŖĒāŃõ»ÆĢś³Įµķ£¬»ÆѧŹ½ĪŖ£ŗFe(OH)3£»
(5)ĀĮ÷·¼ĮÖ÷ŅŖ³É·ÖĪŖAl(OH)2Cl£¬ŌŚ¼ÓČČÕō·¢Ź±»į·¢ÉśĖ®½ā£¬ĪŖ·ĄÖ¹Ė®½āĄūÓĆÅēĪķøÉŌļ£¬¼õÉŁĀĮ÷·¼ĮĖ®½ā£»
(6)Éś³ÉĘųĢåÖŠ£¬±„ŗĶŃĒĮņĖįÄĘæÉĪüŹÕ°±Ęų”¢ČżŃõ»ÆĮņ£¬øßĆĢĖį¼ŲĪüŹÕ¶žŃõ»ÆĮņ£¬×īŗóĪüŹÕµŖĘų”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·Ö×ÓŹ½ĪŖC6H12O2ĒŅæÉŅŌÓėĢ¼ĖįĒāÄĘČÜŅŗ·“Ó¦µÄÓŠ»śĪļ»ÆŗĻĪļ(²»æ¼ĀĒĮ¢ĢåŅģ¹¹)ÓŠ(””””)
A£®5ÖÖ”””””” B£®6ÖÖ”””””” C£®7ÖÖ”””””” D£®8ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅÖŠ±£“ęĻĀĮŠ»ÆѧŅ©Ę·µÄ·½·Ø²»Ķ×µ±µÄŹĒ(””””)
A. ½«AgNO3¾§Ģå·ÅŌŚ×ŲÉ«ŹŌ¼ĮĘæÖŠ
B. NaOHČÜŅŗ±£“ęŌŚ“ųĻš½ŗČūµÄĻøæŚŹŌ¼ĮĘæÖŠ
C. ½šŹō¼Ų”¢ÄĘŗĶ·Ē½šŹō°×Į×±£“ęŌŚĆŗÓĶÖŠ
D. ÅØĻõĖįČÜŅŗ±£“ęŌŚ×ŲÉ«ŹŌ¼ĮĘæÖŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹĀŹµ£¬²»ÄÜÓĆĄÕĻÄĢŲĮŠŌĄķ½āŹĶµÄŹĒ
A£®ĮņĖį¹¤ŅµÖŠ£¬Ōö“óO2µÄÅضČÓŠĄūÓŚĢįøßSO2µÄ×Ŗ»ÆĀŹ
B£®¶Ō2HI£Øg£©![]() H2£Øg£©+I2£Øg£©Ę½ŗāĢåĻµŌö¼ÓŃ¹ĒæŹ¹ŃÕÉ«±äÉī
H2£Øg£©+I2£Øg£©Ę½ŗāĢåĻµŌö¼ÓŃ¹ĒæŹ¹ŃÕÉ«±äÉī
C£®æŖĘōĘ”¾ĘĘæŗó£¬ĘæÖŠĮ¢æĢ·ŗĘš“óĮæÅŻÄ
D£®µĪÓŠ·ÓĢŖµÄ°±Ė®ČÜŅŗ£¬ŹŹµ±¼ÓČČČÜŅŗ£Ø°±Ęų²»»Ó·¢£©ŗóŃÕÉ«±äÉī£Ø×¢£ŗNH3”¤H2OµÄµēĄėŹĒĪüČČ·“Ó¦£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹĀ¹Ź“¦Ąķ²»ÕżČ·µÄŹĒ£Ø £©
A. ²»É÷Åöµ¹¾Ę¾«µĘ£¬Č÷³ö¾Ę¾«ŌŚ×ĄÉĻČ¼ÉÕ£¬Ó¦Į¢¼“ÓĆŹŖÄز¼ĘĖøĒ
B. ½«Ņ»Ńõ»ÆĢ¼ÖŠ¶¾ÕßŅʵ½ĶØ·ē“¦ĒĄ¾Č
C. ŹµŃéŗó£¬Ź£ÓąµÄŅ©Ę·²»ÄÜ·Å»ŲŌĘ棬Ņ²²»ÄÜĖę±ć¶ŖĘś
D. ²»É÷°ŃÅؼī½¦ŌŚĘ¤·ōÉĻ£¬ÓĆ“óĮæĖ®³åĻ“ŗó£¬ŌŁĶæÉĻĢ¼ĖįĒāÄĘČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČ«Éē»į¶¼ŌŚ³«µ¼³ĻŠÅ£¬Č»¶ų×ÜŹĒÓŠŅ»²æ·Ö²»·ØÉĢ··Č“ŌŚ±³µĄ¶ų³Ū£®ČēÓŠŠ©ÉĢ··ĪŖĮĖŹ¹Ņų¶śŌö°×£¬¾ĶÓĆĮņ»Ē£ØČ¼ÉÕĮņ»Ē£©¶ŌŅų¶ś½ųŠŠŃ¬ÖĘ£¬ÓĆÕāÖÖ·½·ØÖĘČ”µÄ½ą°×µÄŅų¶ś¶ŌČĖĢåŹĒÓŠŗ¦µÄ£®ÕāŠ©²»·ØÉĢ··ĖłÖĘČ”Ņų¶śĄūÓƵďĒ£Ø £©
A.SµÄĘư׊Ō
B.SµÄ»¹ŌŠŌ
C.SO2µÄĘư׊Ō
D.SO2µÄ»¹ŌŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĆܱÕČŻĘ÷ÖŠ³äČėµČĪļÖŹµÄĮæµÄAŗĶB£¬Ņ»¶ØĪĀ¶ČĻĀ·¢Éś·“Ó¦A£Øg£©£«xB£Øg£©![]() 2C£Øg£©£¬“ļµ½Ę½ŗāŗó£¬ŌŚ²»Ķ¬µÄŹ±¼ä¶Ī£¬·Ö±šøı䷓ӦµÄŅ»øöĢõ¼ž£¬²āµĆČŻĘ÷ÖŠĪļÖŹµÄĪļÖŹµÄĮæÅØ¶Č”¢·“Ó¦ĖŁĀŹ·Ö±šĖꏱ¼äµÄ±ä»ÆČēĻĀĶ¼ĖłŹ¾,ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
2C£Øg£©£¬“ļµ½Ę½ŗāŗó£¬ŌŚ²»Ķ¬µÄŹ±¼ä¶Ī£¬·Ö±šøı䷓ӦµÄŅ»øöĢõ¼ž£¬²āµĆČŻĘ÷ÖŠĪļÖŹµÄĪļÖŹµÄĮæÅØ¶Č”¢·“Ó¦ĖŁĀŹ·Ö±šĖꏱ¼äµÄ±ä»ÆČēĻĀĶ¼ĖłŹ¾,ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
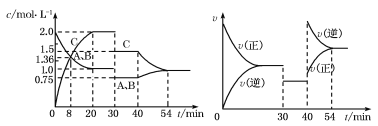
A£®30 min”«40 min¼äøĆ·“Ó¦Ź¹ÓĆĮĖ“߻ƼĮ
B£®·“Ó¦·½³ĢŹ½ÖŠµÄx£½1£¬Õż·“Ó¦ĪŖĪüČČ·“Ó¦
C£®30 minŹ±½µµĶĪĀ¶Č£¬40 minŹ±ÉżøßĪĀ¶Č
D£®8 minĒ°AµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.08 mol”¤L£1”¤min£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀȱ“ĢŲ(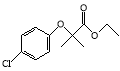 )ŹĒĮŁ“²ÉĻŅ»ÖÖ½µÖ¬æ¹ŃŖĖØŅ©Īļ£¬ĖüµÄŅ»ĢõŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
)ŹĒĮŁ“²ÉĻŅ»ÖÖ½µÖ¬æ¹ŃŖĖØŅ©Īļ£¬ĖüµÄŅ»ĢõŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
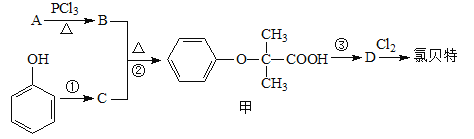
ĢįŹ¾£ŗ¢ń£®Ķ¼ÖŠ²æ·Ö·“Ó¦Ģõ¼ž¼°²æ·Ö·“Ó¦Īļ”¢Éś³ÉĪļŅŃĀŌČ„”£
¢ņ£®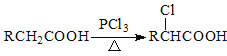
¢ó£®![]()
¢ÅĀȱ“ĢŲµÄ·Ö×ÓŹ½ĪŖ ”£
¢ĘČō8.8 g AÓė×ćĮæNaHCO3ČÜŅŗ·“Ӧɜ³É2.24 L CO2(±ź×¼×“æö)£¬ĒŅBµÄŗĖ“Ź²ÕńĒāĘ×ÓŠĮ½øö·å£¬ŌņAµÄ½į¹¹¼ņŹ½ĪŖ ”£(Ļą¶ŌŌ×ÓÖŹĮæ£ŗH-1”¢C-12”¢O-16)
¢ĒŅŖŹµĻÖ·“Ó¦¢ŁĖłŹ¾µÄ×Ŗ»Æ£¬¼ÓČėĻĀĮŠĪļÖŹ²»ÄÜ“ļµ½ÄæµÄµÄŹĒ (ĢīŃ”Ļī×ÖÄø)”£
a£®Na b£®NaOH c£®NaHCO3 d£®CH3COONa
¢Č·“Ó¦¢ŚµÄ·“Ó¦ĄąŠĶĪŖ £¬Ęä²śĪļ¼×ÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壬Ķ¬Ź±Āś×ćŅŌĻĀĢõ¼žµÄĖłÓŠ¼×µÄĶ¬·ÖŅģ¹¹ĢåÓŠ ÖÖ(²»æ¼ĀĒĮ¢ĢåŅģ¹¹)”£
¢Ł 1£¬3£¬5-ȿȔ“ś±½£»
¢Ś ŹōÓŚõ„ĄąĒŅ¼ČÄÜÓėFeCl3ČÜŅŗĻŌ×ĻÉ«£¬ÓÖÄÜ·¢ÉśŅų¾µ·“Ó¦£»
¢Ū 1 moløĆĶ¬·ÖŅģ¹¹Ģå×ī¶ąÄÜÓė3 mol NaOH·“Ó¦”£
¢ÉŠ“³öBÓė×ćĮæNaOHČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»Ģå»żæɱäµÄĆܱÕČŻĘ÷ÖŠ£¬¼ÓČėŅ»¶ØĮæµÄX”¢Y£¬·¢Éś·“Ó¦mX£Øg£©![]() nY£Øg£© ¦¤H£½Q kJ/mol”£·“Ó¦“ļµ½Ę½ŗāŹ±£¬YµÄĪļÖŹµÄĮæÅضČÓėĪĀ¶Č”¢ĘųĢåĢå»ż£ØČŻĘ÷ČŻ»ż£©µÄ¹ŲĻµČēĻĀ±ķĖłŹ¾£ŗ
nY£Øg£© ¦¤H£½Q kJ/mol”£·“Ó¦“ļµ½Ę½ŗāŹ±£¬YµÄĪļÖŹµÄĮæÅضČÓėĪĀ¶Č”¢ĘųĢåĢå»ż£ØČŻĘ÷ČŻ»ż£©µÄ¹ŲĻµČēĻĀ±ķĖłŹ¾£ŗ
ĘųĢåĢå»ż/L c £ØY£©/mol”¤L£1 ĪĀ¶Č/”ę | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1.20 | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®m>n
B£®Q<0
C£®ĪĀ¶Č²»±ä£¬Ń¹ĒæŌö“ó£¬YµÄÖŹĮæ·ÖŹż¼õÉŁ
D£®Ģå»ż²»±ä£¬ĪĀ¶ČÉżøߣ¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅʶÆ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com