
(5分)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:

(1)属于阴离子结构示意图的是 (填字母编号)。
(2)性质最稳定的原子是 (填字母编号)。
(3)元素D的单质在B2中燃烧,该产物的化学式 。
(4)在核电荷数1-18的元素内,列举一个与C原子的电子层结构相同的离子,写出离子的符号 。
(5)写出化合物DAB在水溶液中的电离方程式 。
(1) A (2) C (3) Na2O2 (4) F-(Na+等合理均可) (5) NaClO=Na++ClO-
【解析】
试题分析:根据结构示意图知道A是Cl-结构示意图,B是O原子结构示意图,C是Ne原子结构示意图,D是Na原子结构示意图,E是Mg2+结构示意图。(1)是阴离子结构示意图的是Cl-结构示意图,选A;(2)Ne是惰性气体,性质最稳定,选C;(3)D是Na,,B是O,Na在O2中燃烧产物是Na2O2(4)Ne是10电子体,1-18的元素内10电子体的离子有O2-、F- 、Na +、Mg2+等。(5)根据上述推断化合物DAB是NaClO,是强电解质,在水溶液中的电离方程式为:NaClO=Na++ClO-
考点:原子结构示意图和基本的化学反应。


 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源:2014-2015河南省许昌市四校高一上学期第三次联考化学试卷(解析版) 题型:选择题
下列有关溶液的说法正确的是
A.将质量分数为40%(密度为1.43 g·cm-3)的NaOH溶液与等体积水混合,所得溶液中溶质的质量分数是20%
B.要配制浓度为0.25 mol·L-1的NaOH溶液480 mL,应称量4.8 g NaOH在250 mL的烧杯中溶解,冷却,再转移到500 mL容量瓶中,洗涤、转移、定容
C.配制一定物质的量浓度的溶液,定容时俯视刻度线导致所配浓度偏高
D.配制NaOH溶液,在烧杯中溶解NaOH后未冷却至室温就转移到容量瓶中,溶液浓度偏低
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省建人高复高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列溶液中有关物质的量浓度关系正确的是
A.NaHSO3溶液呈酸性,则有:c(Na+)>c(HSO3-)>c(SO32-)>c(H+)>c(OH-)
B.pH相等的CH3COONa和Na2CO3两种溶液:c(CH3COONa)<c(Na2CO3)
C.强酸HA溶液与弱碱MOH溶液混合后溶液呈中性,则有:c(M+)=c(A-)
D.0.1 mol·L-1的 NaHA 溶液pH=1则有c(Na+)=c(H2A)+c(HA-)+c(A2-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省建人高复高三上学期第三次月考化学试卷(解析版) 题型:选择题
含有下列各组离子的溶液中,通入(或加入)过量的某种物质后仍能大量共存的是
A.H+、Ba2+、Fe3+、NO3―,通入SO2气体
B.Ca2+、Cl―、K+、H+,通入CO2气体
C.Al(OH)4-、Na+、Br-、SO42-,通入CO2气体
D.HCO3―、 Na+、I― 、 HS―,加入AlCl3溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期第三次月考化学试卷(解析版) 题型:计算题
(6分)为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液。下图是医院病人输液使用的一瓶质量分数为6%的葡萄糖(C6H12O6)注射液标签,

请认真观察标签上所列内容后计算:
(1)该溶液的物质的量浓度为 mol·L-1。
(2)该溶液的密度为 g·mL-1(精确到0.1g)。
(3)如果从该瓶中取出75g葡萄糖注射液,将其变为15%的注射液,需要加入 ______g葡萄糖固体(精确到0.1g)。
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.Cu与FeCl3溶液反应:Cu+ Fe3+= Cu2++ Fe2+
B.碳酸钙溶于稀盐酸:CO32- + 2H+ = H2O + CO2↑
C.金属钠与水反应:2Na+2 H2O=2Na ++2OH- + H2↑
D.氯气溶于水:Cl2 + H2O = 2H+ + ClO- + Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期第三次月考化学试卷(解析版) 题型:选择题
海洋是一个巨大的宝藏,期待着人们的开发和利用,下列有关海水综合利用的说法正确的是
A.从海水中提取溴单质只有物理变化发生
B.从海水制海盐主要是通过化学变化完成
C.电解熔融的氯化镁可制备镁和氯气
D.电解氯化钠溶液可以制得钠和氯气
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二上学期第三次月考化学试卷(解析版) 题型:选择题
已知:相同温度下Ka(HF)﹥Ka(HCN)。现有物质的量浓度和体积均相同的NaF和NaCN两种溶液,已知前者溶液中所含离子数目为n1,后者溶液中所含离子数目为n2,下列关系正确的是
A.溶液pH:NaF﹥NaCN B.n1 ﹥ n2 C.n1 ﹤ n2 D.c(F-)﹤c(CN-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省乐山市高三第一次调查研究考试理综化学试卷(解析版) 题型:填空题
(16分)
二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用下图所示装置模拟工业制取并收集ClO2。

(1)A中反应产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式: 。
(2)A必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、 ;B也必须添加温度控制装置,应该是 (选填“冰水浴”或“热水浴”)装置。
(3)反应后在装置C中可得NaClO2溶液。已知NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2·3H2O,在温度高于38℃时析出晶体是NaClO2。根据下图所示的NaClO2的溶解度曲线,
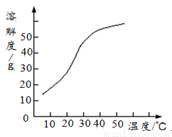
请补充从NaClO2溶液中制得NaClO2的操作步骤:① ;② ;③洗涤;④干燥。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样;量取V1 mL试样加入到锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用c mol·L—1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知2 Na2S2O3 + I2 = Na2S4O6 + 2NaI)
①滴定过程中,至少须进行两次平行测定的原因是 。
②原ClO2溶液的浓度为 g / L(用步骤中的字母代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com