
| A. | 用纯碱溶液洗涤沾有油污的器具 | |
| B. | 用食醋除去热水瓶胆中积存的水垢 | |
| C. | 用米汤检验加碘盐中含有碘 | |
| D. | 用灼烧并闻气味的方法区分化纤物质与纯毛织物 |
分析 A.纯碱水解生成NaOH和碳酸氢钠,NaOH促进油脂水解;
B.水垢的主要成分是碳酸钙,碳酸钙和醋酸反应生成醋酸钙、水和二氧化碳;
C.碘遇淀粉试液变蓝色;
D.蛋白质灼烧有烧焦羽毛的气味.
解答 解:A.纯碱水解生成NaOH和碳酸氢钠,NaOH促进油脂水解,所以可以用纯碱溶液洗涤沾有油污的器具,热的纯碱溶液效果更好,故A正确;
B.水垢的主要成分是碳酸钙,碳酸钙和醋酸反应生成醋酸钙、水和二氧化碳,所以可以用食醋除去热水瓶胆中积存的水垢,故B正确;
C.碘遇淀粉试液变蓝色,加碘盐中加的是KIO3而不是碘单质,所以加碘盐中加入淀粉试液不变蓝色,故C错误;
D.蛋白质灼烧有烧焦羽毛的气味,毛织物的主要成分是蛋白质,化纤维质主要成分不是蛋白质,所以用灼烧并闻气味的方法区分化纤物质与纯毛织物,故D正确;
故选C.
点评 本题考查化学实验方案评价,为高频考点,明确实验原理、物质性质是解本题关键,涉及物质鉴别、物质应用,物质鉴别时利用物质性质差异性,侧重考查学生分析评价能力,题目难度不大.


科目:高中化学 来源: 题型:解答题

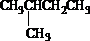

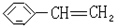 苯乙烯
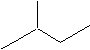
苯乙烯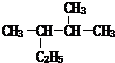 2,3-二甲基戊烷
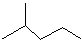
2,3-二甲基戊烷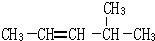 4-甲基-2戊烷
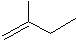
4-甲基-2戊烷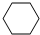 环己烷.
环己烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 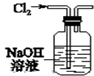 用图装置除去Cl2中混有的少量HCl | |
| B. | 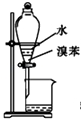 用图装置分离水和溴苯的混合物 | |
| C. | 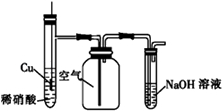 用图装置制备并收集NO气体 | |
| D. | 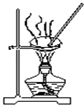 用图装置蒸干AlCl3饱和溶液制备AlCl3晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
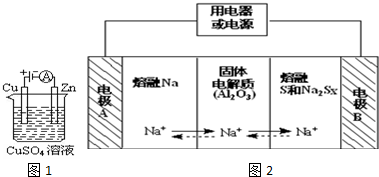
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乳酸薄荷醇酯( 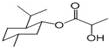 )仅能发生水解、氧化、消去反应 )仅能发生水解、氧化、消去反应 | |
| B. | 乙醛和丙烯醛( )不是同系物,它们与氢气充分反应后的产物也不是同系物 )不是同系物,它们与氢气充分反应后的产物也不是同系物 | |
| C. | 油脂在碱性条件下水解生成高级脂肪酸和甘油 | |
| D. | CH3COOCH2CH3 与CH3CH2COOCH3 互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠与稀盐酸 | B. | 过氧化钠与二氧化碳 | ||
| C. | 氢氧化钠与二氧化碳 | D. | 钠与氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3、PH3、AsH3 | B. | SiH4、PH3、H2S | C. | HI、HBr、HCl | D. | H2S、HCl、AsH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
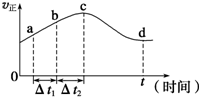 过氧化氢和臭氧都是常见的绿色氧化剂,工业生产中有着重要用途.
过氧化氢和臭氧都是常见的绿色氧化剂,工业生产中有着重要用途.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com