
| A、两者都为s-s σ键 |
| B、两者都为p-p σ键 |
| C、前者为p-p σ键,后者为s-p σ键 |
| D、前者为s-s σ键,后者为s-p σ键 |
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸和磷酸(H3PO4)的摩尔质量不相等 |
| B、18 g水中含有1 mol水分子 |
| C、O2的摩尔质量等于其相对分子质量 |
| D、1mol CO的质量是28 g?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当正、逆反应的速率同时改变,则平衡一定会发生移动 |
| B、只要能加快正反应速率,一定能使化学平衡向正反应方向移动 |
| C、对于有颜色的平衡体系,当颜色发生变化则平衡一定发生移动 |
| D、温度的改变对任一化学反应体系的反应速率与平衡一定都有影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg HCl H2CO3 CaO |
| B、O2 NaOH H2SO4 SO2 |
| C、NO CH4 NaOH CaO |
| D、NO KCl HNO3 SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有相同氧原子数的SO2和CO的质量相等 |
| B、等物质的量浓度的稀硫酸溶液与盐酸中的H+浓度相等 |
| C、等温等压下,2mol N2和1mol CO的密度相等 |
| D、100mL 2mol/L的NaOH溶液取出50mL,剩余溶液浓度为1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、二氧化碳的电子式: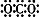 | ||
B、S2-的粒子结构示意图: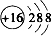 | ||
C、甲烷分子的结构式: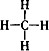 | ||
D、R2+离子核外有a个电子,b个中子,R原子克表示为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、B和C可能都是气体 |
| B、B和C一定都是气体 |
| C、若C为固体,则B一定是气体 |
| D、不可能B为固体,C为气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com