
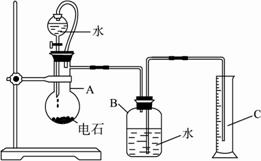
图12-4
(1)烧瓶要干燥,放入电石后应塞紧橡皮塞,这是为了 。装置B和C的作用是 。?
(2)从分液漏斗中向烧瓶里滴加水的操作方法是 。?
(3)所用的电石质量不能太多,否则 ;也不能太少,否则 。若容器B的容积为250 mL,则所用的电石质量应在______________g左右(选填:0.30,0.60,1.00,1.50,2.00)。
科目:高中化学 来源: 题型:阅读理解
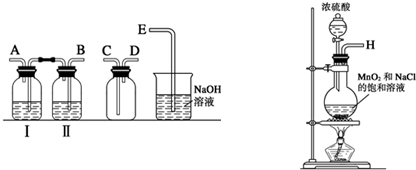
 某化学兴趣小组为探究铜跟浓硫酸的反应,如图所示装置进行有关实验.
某化学兴趣小组为探究铜跟浓硫酸的反应,如图所示装置进行有关实验.
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
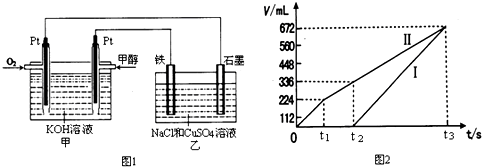
| 容器 | A | B |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| CH3OH(g)浓度(mol?L-1) | c1 | c2 |
| 反应能量变化 | 放出29.4kJ | 吸收akJ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
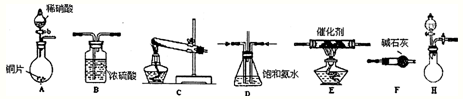
| 实验编号 | T/℃ | NO初始浓度 mol?L-1 |
CO初始浓度 mol?L-1 |
催化剂的比表面积 ㎡?g-1 |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
| 试剂组合序号 | 固体试剂(g) | NH3体积(mL) | |
| a | 12.0g Ca(OH)2(过量) | 10.8g NH4Cl | 2688 |
| b | 10.8g(NH4)2SO4 | 2728 | |
| c | 12.0g NaOH(过量) | 10.8g NH4Cl | 3136 |
| d | 10.8g(NH4)2SO4 | 3118 | |
| e | 12.0g CaO(过量) | 10.8g NH4Cl | 3506 |
| f | 10.8g(NH4)2SO4 | 3584 | |
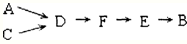
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作 | 现象 |
| 取4g漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
 |
ⅰ.液面上方出现雾状物 ⅱ.稍后,出现浑浊,溶液变为黄绿色 ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com