
 ,化合物C所含官能团的名称为羧基.
,化合物C所含官能团的名称为羧基. $→_{△}^{浓硫酸}$R-CH=CH2+H2O,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑.
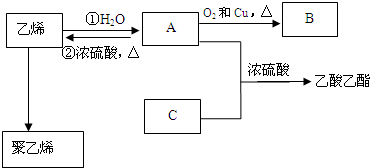
$→_{△}^{浓硫酸}$R-CH=CH2+H2O,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑.分析 根据题中各物质转化关系,乙烯与水发生加成反应得A为CH3CH2OH,CH3CH2OH催化氧化得B为CH3CHO,A和C在浓硫酸作用下生成乙酸乙酯,所以C为CH3COOH,乙烯发生加聚反应得聚乙烯,据此答题.
解答 解:根据题中各物质转化关系,乙烯与水发生加成反应得A为CH3CH2OH,CH3CH2OH催化氧化得B为CH3CHO,A和C在浓硫酸作用下生成乙酸乙酯,所以C为CH3COOH,乙烯发生加聚反应得聚乙烯,
(1)聚乙烯的结构简式为: ,C为CH3COOH,C所含官能团的名称为羧基,
,C为CH3COOH,C所含官能团的名称为羧基,
故答案为: ;羧基;
;羧基;
(2)A→B的化学方程式为2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O,反应类型:氧化反应,
故答案为:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O;氧化反应;
(3)根据题中的信息可知,反应②的反应方程式为CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑,
故答案为:CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑;
(4)乙酸乙酯有一种同分异构体D,D也属于酯类,并且可以跟新制Cu(OH)2悬浊液混合煮沸生成砖红色沉淀,则D中含有醛基,应为甲酸某酸,所以D的一种结构简式为HCOOCH(CH3)2或HCOOCH2CH2CH3,
故答案为:HCOOCH(CH3)2或HCOOCH2CH2CH3.
点评 本题主要考查常见有机物的性质与推断,涉及烯、醇、醛、羧酸、酯的性质,难度不大,注意有机基础知识的灵活运用.


科目:高中化学 来源: 题型:选择题
| A. | Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-═2Fe2++I2+3H2O | |
| B. | 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO${\;}_{4}^{-}$+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| D. | 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸能溶解除金、铂外的大多数金属 | |
| B. | 汽车尾气中含有NO和CO | |
| C. | 浓氨水可检验氯气管道漏气 | |
| D. | 制取二氧化氮时,常用水吸收尾气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Y | Z | ||
| M | X |
| A. | 原子半径Z<M | |
| B. | 非金属性:X<Z | |
| C. | M元素最高价氧化物对应水化物具有两性 | |
| D. | Y的最高价氧化物对应水化物的酸性比X的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 可用来制备抗凝血药,通过如图路线合成:
可用来制备抗凝血药,通过如图路线合成:
 +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O.
+CH3COONa+CH3OH+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com