


���� ��1���ٸ���ͼ2��֪�������¶Ⱥ�CO��ת���ʼ�С��˵���÷�ӦΪ���ȷ�Ӧ����߷�ӦCO ��g��+2H2��g��?CH3OH ��g����һ����̼��ת���ʣ���Ӧ��ʹƽ�����������ƶ�������Ӱ�컯ѧƽ������ؽ����жϣ�
�ڸ��ݻ�ѧƽ������ʽ��ƽ�ⳣ������ʽ���м��㣻
�۸÷�Ӧ��Ӧǰ����������ʵ������䣬����������䣬����ϵѹǿ�㶨�����Ⱥ����ܱ���������ϵ�¶��淴Ӧ���б仯���淴Ӧ���з�Ӧ���Ũ�Ƚ��ͣ���ͼ��֪��c����ǰ����Ӧ��������˵������ӦΪ���ȷ�Ӧ��c���Ժ�Ӧ����Ӧ���ʽ��ͣ�Ӧ��Ũ��Ӱ����¶�Ӱ�����ͼΪ����Ӧ������ʱ��仯��˵����Ӧδ����ƽ�⣻
��2��ȼ�ϵ�صĸ�������ȼ�Ϸ���ʧ���ӵ�������Ӧ��ȷ����������Ȼ��ȷ���缫����������������ԭ��Ӧ��д�缫��Ӧʽ��
��3�����ݼ״���ȼ���ȼ�������ļ״������ʵ������ٸ��ݻ��ϼ۱仯�����ת�Ƶ��ӵ����ʵ�����
��4�������Ȼ�ѧ����ʽ���ø�˹���ɼ��㷴Ӧ�Ȳ���д�Ȼ�ѧ����ʽ��
��� �⣺��1����A������ͼ2��֪�������¶Ⱥ�CO��ת���ʼ�С�����Բ��ܸ��²��������CO��ת���ʣ���A����
B���������������Ӱ�췴Ӧ���ʣ�����Ӱ�컯ѧƽ�⣬��CO��ת���ʲ��䣬��B����
C������CO��Ũ�ȣ�CO��ת���ʻ��С����C����
D������������Ũ�ȣ�ƽ�����������ƶ�����CO��ת��������D��ȷ��
E��������״���������Ũ�ȼ�С��ƽ�����������ƶ���CO��ת��������E��ȷ��
�ʴ�Ϊ��D E��
����ѹǿΪ0.1MPa�����£��ݻ�ΪV L���ܱ�������a mol CO��2a mol H2�ڴ��������·�Ӧ���ɼ״�����
CO��g��+2H2��g���TCH3OH��g��
��ʼŨ�ȣ�$\frac{a}{V}$ $\frac{2a}{V}$ 0
�仯Ũ�ȣ�$\frac{a}{2V}$ $\frac{a}{V}$ $\frac{a}{2V}$
ƽ��Ũ�ȣ�$\frac{a}{2V}$ $\frac{a}{V}$ $\frac{a}{2V}$
����¶��¸÷�Ӧ��ƽ�ⳣ��Ϊ��K=$\frac{\frac{a}{2V}}{��\frac{a}{2V}������{\frac{a}{V}��}^{2}}$=$\frac{{V}^{2}}{{a}^{2}}$��
��P1�£�100��ʱ��CH3OH��g���TCO��g��+2H2��g����Ӧ��ƽ�ⳣ���ͷ�ӦCO��g��+2H2��g���TCH3OH��g����K��Ϊ���������Ը÷�Ӧ��ƽ�ⳣ��K=$\frac{{a}^{2}}{{V}^{2}}$��
�ʴ�Ϊ��K=$\frac{{a}^{2}}{{V}^{2}}$��
��A����ѧƽ��״̬�ı�־�Ǹ����ʵ�Ũ�Ȳ��ٸı䣬��ʵ��������Ӧ���ʵ����淴Ӧ���ʣ�c���Ӧ������Ӧ������Ȼ���ڸı䣬��һ��δ��ƽ�⣬��A����
B��a��bʱ����Ӧ�������ӣ���Ӧ��Ũ����ʱ�䲻�ϼ�С����B����
C����a��c����Ӧ��������֮������Ӧ���ʼ�С��˵����Ӧ�տ�ʼʱ�¶����߶�����Ӧ���ʵ�Ӱ�����Ũ�ȼ�С������Ӧ���ʵ�Ӱ�죬˵���÷�ӦΪ���ȷ�Ӧ������Ӧ������������������������������C��ȷ��
D�����ŷ�Ӧ�Ľ��У�����Ӧ����Խ�죬���ĵĶ��������Խ�࣬SO2��ת���ʽ�������SO2����������a��b��С��b��c�Σ���D����
�ʴ�Ϊ��C��
��2����ͼ��֪��ȼ�ϵ�صĸ�������ȼ�Ϸ���ʧ���ӵ�������Ӧ��ȼ�ϵ����H2����ԭ�����ڸ���������Ӧ������Ϊ�������������Ϸ����缫��ӦΪ2H++O2+2e-=H2O2��
�ʴ�Ϊ��2H++O2+2e-=H2O2��
��3����֪�״���ȼ����Ϊ725.76kJ/mol����������һ�����ļ״���ȫȼ������Һ̬ˮ�ͷų���1451.52kJ�������������ļ״������ʵ���Ϊ��$\frac{1451.52kJ}{725.76kJ/mol}$=2mol���״���CԪ�صĻ��ϼ�Ϊ-2�ۣ���Ӧ������+4�۵Ķ�����̼������������ļ״�ȼ�ϵ���������Ͽ��ṩ���ӵ����ʵ���Ϊ��2mol��[4-��-2��]=12mol��
�ʴ�Ϊ��12��
��4����2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H=-1275.6kJ/mol
��2CO ��g��+O2��g��=2CO2��g����H=-566.0kJ/mol
��H2O��g��=H2O��l����H=-44.0kJ/mol
���ݸ�˹���ɢ�-��+�ۡ�4�õ��״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��2CH3OH��l��+2O2��g��=2CO ��g��+4H2O��l����H=-885.6KJ/mol��
�õ��Ȼ�ѧ����ʽΪ��CH3OH��l��+O2��g��=CO ��g��+2H2O��l����H=-442.8KJ/mol��
�ʴ�Ϊ��CH3OH��l��+O2��g��=CO ��g��+2H2O��l����H=-442.8KJ/mol��
���� ���⿼���˽�Ϊ�ۺϣ��漰ԭ���ԭ������˹�������Ȼ�ѧ����ʽ�е�Ӧ�á���ѧƽ�⼰��Ӱ�졢��ѧƽ�ⳣ���ļ����֪ʶ��ע��Ի���֪ʶ�İ��գ�����֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ���ѧ���ķ�����������������ѧ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SO4 | B�� | HCl | C�� | KMnO4 | D�� | HNO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
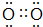 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HSO3-����Һ�з���ˮ�⣺HSO3-+H2O?SO32-+H3O+ | |
| B�� | ��NaClO��Һ��ͨ������SO2��2ClO��+SO2+H2O�TSO32��+2HClO | |
| C�� | ��������Һ�Լ��ԣ�C6H5O-+H2O?C6H5OH+OH- | |
| D�� | ���Ե缫���MgCl2��Һ��Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$ OH-+Cl2��+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ��ˮ | B�� | CO | C�� | ���� | D�� | C2H5OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��B��ͬ���ڵ�һ��������С��Ԫ�أ�C�������������δ�ɶԵ��ӣ�E����Χ�����Ų�ʽΪ3d64s2���ش��������⣺
��B��ͬ���ڵ�һ��������С��Ԫ�أ�C�������������δ�ɶԵ��ӣ�E����Χ�����Ų�ʽΪ3d64s2���ش��������⣺ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȩ�ķ���ʽ��C2H4O | B�� | ���Ľṹ��ʽ��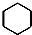 | ||
| C�� | ��Ȳ�Ľṹ��ʽ��CH��CH | D�� | �Ҵ��Ľṹ��ʽ��C2H5OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������е����Ų�ʽ��ԭ���У���1s22s22p63s2����1s22s22p63s23p1����һ�����ܣ��٣��� | |
| B�� | ijԪ����̬��̬ԭ�ӵ������ܣ�kJ•mol-1���ֱ�Ϊ738��1451��7733��10540��13630��17995��21703��������������Ӧʱ�������ɵ���������X3+ | |
| C�� | �������м۵����Ų�ʽ��ԭ���У���3s23p2��2s22p3��ԭ�Ӱ뾶�٣��� | |
| D�� | Na��P��Cl����Ԫ�صĵ縺���������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com