
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在这些元素中,金属性最强的元素是_______,最活泼的非金属元素是_______;
(2)化学性质最不活泼的元素是__________,其原子的原子结构示意图为_____________;
(3)元素的最高价氧化物对应的水化物中酸性最强的是______________,碱性最强的是____________,呈两性的氢氧化物是____________________;
(4)③~⑦元素中,原子半径最大的是________,原子半径最小的是____________;
(5)在⑦与⑩的单质中,化学性质较活泼的是_____________,可用什么化学反应说明该事实(写出反应的化学方程式)____________________。
【答案】K F Ar 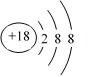 HClO4 KOH Al(OH)3 Na Cl Cl2 2NaBr+Cl2=2NaCl+Br2
HClO4 KOH Al(OH)3 Na Cl Cl2 2NaBr+Cl2=2NaCl+Br2
【解析】
(1)根据元素周期表中金属性和非金属性的递变规律来回答;
(2)化学性质最不活泼的元素应该是稀有气体元素;根据原子结构示意图的写法来写;
(3)根据元素周期律的知识来回答;
(4)同一周期元素从左到右原子半径减小;
(5)同一主族从上到下单质的氧化性逐渐减弱,可以根据单质间的置换反应来证明。
由元素在周期表中的位置可知,①为N,②为F,③为Na,④为Mg,⑤为Al,⑥为Si,⑦为Cl,⑧为Ar,⑨为K,⑩为Br;
(1)周期表中,同周期从左到右失电子能力逐渐减弱,得电子能力逐渐增强,同主族从上到下失电子能力逐渐增强,得电子能力逐渐减弱,所以失电子能力最强的是K,得电子能力最强的是F,得电子能力强则元素的非金属性就强;
答案:K;F;
(2)上述元素中只有Ar原子的最外层电子数为8,性质不活泼,原子结构示意图为: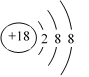 ;
;
答案: Ar 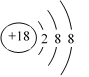
(3)根据元素周期律:周期表中,同周期从左到右失电子能力逐渐减弱,得电子能力逐渐增强,元素非金属性逐渐增强,同主族从上到下失电子能力逐渐增强,得电子能力逐渐减弱,元素非金属性逐渐减弱,上述元素中Cl的最高价氧化物对应的水化物的酸性最强,该酸为HClO4,K的金属性最强,则KOH的碱性最强,Al(OH)3为两性氢氧化物;
答案:HClO4;KOH;Al(OH)3;
(4)同一周期,元素原子半径从左到右减小,则Na的原子半径最大,Cl的最小;答案:Na;Cl
(5)同主族从上到下,单质的氧化性逐渐增强,所以氯气的氧化性强于溴单质,可以通过水溶液中的置换反应来证明,即2NaBr+Cl2=2NaCl+Br2;
答案:Cl2;2NaBr+Cl2=2NaCl+Br2


科目:高中化学 来源: 题型:
【题目】相同条件下,下列物质在水中的溶解度最大的是
A. C17H35COOH B. CH3COOCH3 C. ![]() D. HOCH2CH(OH)CH2OH
D. HOCH2CH(OH)CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置.下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu
C. 无论a和b是否连接,铁片均会溶解
D. a和b用导线连接后,Fe片上发生还原反应,溶液中的Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多个氨基酸分子缩合成含两条肽链的蛋白质时,相对分子量减少了900,由此可推知:此蛋白质分子所含的氨基酸数和肽键数分别是( )
A. 52、52 B. 50、50 C. 52、50 D. 50、49
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用如图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件。下列判断正确的是

A. e、f两管中的试剂可以分别是浓氨水和NaOH固体
B. 玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
C. c、d两根导管都必须插入BaCl2溶液中,保证气体与Ba2+充分接触
D. Y形管乙中产生的为氧化性气体,将BaSO3氧化为BaSO4沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母x表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断回答下列问题:
(1)f在周期表中的位置是__________。
(2)比较d、e常见离子的半径大小(用化学式表示,下同):_______>__________;________比较g、h的最高价氧化物对应水化物的酸性强弱:_______>__________。____________
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:_________________。
(4)写出e的单质在足量d2中燃烧反应的化学方程式:____________________________。
(5)上述元素可组成盐R:zx4f(gd4)2。向盛有10 mL 1 mol·L-1R溶液的烧杯中逐滴加入1 mol·L-1NaOH溶液,沉淀的物质的量随加入NaOH溶液体积的变化示意图如下:
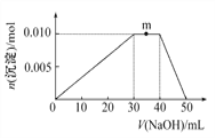
①写出m点反应的离子方程式:____________________________。
②若在R溶液中改加20 mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到的滤液用 NaHCO3溶液处理,测得溶液pH、n[Al(OH)3]随加入NaHCO3溶液体积变化的曲线如下图所示。下列有关说法不正确的是
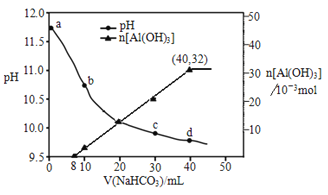
A. 生成沉淀的离子方程式为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-
B. b 点与c点溶液所含微粒种类相同
C. a 点溶液中大量存在的离子是Na+、AlO2-、OH-
D. NaHCO3溶液的物质的量浓度为0.8mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烧硫酸铝铵晶体,发生的主要反应为4[NH4Al(SO4)2·12H2O] ![]() 2A12O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过下图所示的装置(假设试剂均过量)。下列说法正确的是
2A12O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过下图所示的装置(假设试剂均过量)。下列说法正确的是

A. 反应中硫元素既体现氧化性又体现还原性
B. 装置Ⅰ中可以观察到出现白色沉淀,其主要成分是BaSO4和BaSO3
C. 装置Ⅱ中可以观察到高锰酸钾紫色褪去
D. 将装置Ⅰ、Ⅱ顺序交换,仍能观察到相同的现象
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com