
| A、1 mol Na2O2晶体中共含有4NA个离子 |
| B、常温常压下16 g O2和O3混合气体含有NA个氧原子 |
| C、0.1 mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 |
| D、17 g的氢氧根离子中含有的电子数为9NA |
| m |
| M |
| m |
| M |
| 16g |
| 16g/mol |
| m |
| M |
| 17g |
| 17g/mol |


科目:高中化学 来源: 题型:
| A、0.5×(10-14+10-12) mol?L-1 |
| B、5×(10-15+10-11) mol?L-1 |
| C、2.0×10-1 mol?L-1 |
| D、2.0×10-14 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在标准状况下,2.24 L H2O中含有0.1 NA个水分子 |
| B、0.1mol/LNaCl溶液中含有Na+数为0.1NA |
| C、1molFe与足量盐酸完全反应,Fe失去的电子数为2NA |
| D、在常温下,1molH2含有的原子数一定不是2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol H2SO4与1 mol Ba(OH)2完全中和所放出的热量为中和热 |
| B、中和反应都是放热反应,一定条件下二氧化碳被碳还原是吸热反应 |
| C、在101 kPa时,1 mol碳燃烧所放出的热量一定叫碳的燃烧热 |
| D、CO燃烧是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
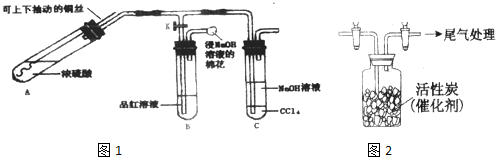
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 实验内容 | 实验目的 |
| A | 室温下,使用pH计测定浓度均为0.1mol/L NaClO溶液和CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| B | 室温下,向两支装有同体积同浓度H2O2溶液的试管中,分别加入3滴同浓度的 CuSO4、FeSO4溶液 | 比较CuSO4、FeSO4作为催化剂对H2O2分解速率的影响 |
| C | 向0.1mol/L AgNO3溶液中滴加0.1mol/L NaCl溶液,至不再有白色沉淀生成,再向其中滴入0.1mol/L KI溶液,观察沉淀颜色变化 | 比较AgCl、AgI的溶解度相对大小. |
| D | 向含有少量FeCl3的MgCl2酸性溶液中加入足量Mg(OH)2,加热并搅拌,过滤 | 除去MgCl2酸性溶液中含有的少量FeCl3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com