
【题目】12mL浓度为0.10molL-1的Na2SO3溶液,恰好与10mL浓度为0.04molL-1的K2Cr2O7溶液完全反应,已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
A. +5
B. +4
C. +3
D. +2
科目:高中化学 来源: 题型:
【题目】【2015福建理综化学】纯净物X、Y、Z转化关系如右图所示,下列判断正确的是 ( )

A.X可能是金属铜
B.Y不可能是氢气
C.Z可能是氯化钠
D.Z可能是三氧化硫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应(表内物质均为反应物)刚开始时,放出H2的速率最大的是( )
编号 | 金属(粉末状) | 物质的量 | 酸的浓度 | 酸的体积 | 反应温度 |
A | Mg | 0.1mol | 6mol/L硝酸 | 10mL | 60℃ |
B | Mg | 0.1mol | 3mol/L盐酸 | 10mL | 30℃ |
C | Fe | 0.1mol | 3mol/L盐酸 | 10mL | 60℃ |
D | Mg | 0.1mol | 3mol/L盐酸 | 10mL | 60℃ |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【加试题】氮及其化合物在生活和生产中应用广泛。
(1)N2O是一种强大的温室气体,在一定条件下,其分解的化学方程式为:2N2O(g)=2N2(g)+O2(g) ΔH<0,你认为该反应的逆反应是否自发进行,请判断并说明理由___________。
某研究小组为针对N2O的分解进行研究,常温下,在1L恒容容器中充入0.100mol N2O气体,加热到一定温度后使之反应,请画出容器中气体的总浓度c(总)随时间t变化的总趋势图。_____________
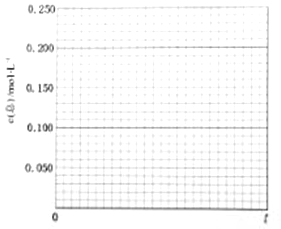
(2)①N2O5是一种新型硝化剂。工业上可用N2O4通过电解制备N2O5,阴、阳极室之间用质子交换膜隔开,两极电解液分别为稀硝酸溶液和溶有N2O4的无水硝酸,用惰性电极电解时,生成N2O5极室的电极反应式为_____________。
②已知,一定条件下有下列反应:
Ⅰ2N2O5(g)![]() 4NO2(g)+ O2(g) ΔH1
4NO2(g)+ O2(g) ΔH1
Ⅱ2NO2(g)![]() 2NO(g)+ O2(g) ΔH2
2NO(g)+ O2(g) ΔH2
Ⅲ2NaOH(aq)+N2O5(g)=2NaNO3(aq)+H2O(1) ΔH3
写出NO和O2的混合物溶于NaOH溶液生成硝酸盐的热化学方程式___________。
在容积为2L的恒容密闭容器中充入1.00mol N2O5,假设在T℃时只发生反应Ⅰ、Ⅱ,若达到平衡状态后O2为1.00mol,NO2为0.400mol,则T℃时反应Ⅰ的平衡常数的值为_________。
(3)NH3和Cr2O3固体在高温下可以制备多功能材料CrN晶体,其反应为Cr2O3(s)+2NH3(g) ![]() 2CrN(s)+3H2O(g)。在800℃时,为降低相同时间内收集到的粗产品中氧的含量,通过提高反应器中NH3(g)流量的工艺手段达成,请解释可能的原因___________。
2CrN(s)+3H2O(g)。在800℃时,为降低相同时间内收集到的粗产品中氧的含量,通过提高反应器中NH3(g)流量的工艺手段达成,请解释可能的原因___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性:H2SO3>H2CO3>HSO3->HCO3-。某无色溶液Y可能含有Na+、Fe3+、Ba2+、NH4+、Cl-、SO42-、HCO3-、HSO3-中的几种离子,溶液中阳离子浓度相同。为了确定其组成,某同学进行了如下实验(假设气体均全部逸出,忽略H2O2的分解)。
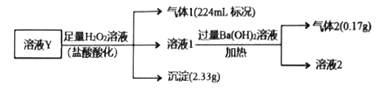
下列说法不正确的是
A. 溶液Y中一定不存在Fe3+、SO42-
B. 溶液Y中肯定存在HCO3-、HSO3-、Ba2+、NH4+
C. 溶液Y中一定含有Cl-,且n(Cl-)=0.01mol
D. 溶液Y中可能存在Na+,为确定其是否存在,可取溶液1通过焰色反应实验验证
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物不能由CH2═CH2通过加成反应制取的是( )
A.CH3CH2Cl
B.CH2Cl﹣CH2Cl
C.CH3﹣CH2OH
D.CH3﹣COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在饱和Mg(OH)2溶液中,c(OH-)=1.0×10-4 mol·L-1。若往该溶液中加入NaOH溶液,使溶液的c(OH-)变为原来的10倍,则Mg(OH)2的溶解度在理论上将
A.变为原来的10-3倍 B.变为原来的10-2倍
C.变为原来的10倍 D.不发生变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com