
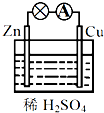
| A、锌棒为正极 |
| B、铜棒上发生还原反应 |
| C、正极反应为Cu-2e-=Cu2+ |
| D、电流从锌棒经外电路流向铜棒 |
科目:高中化学 来源: 题型:
| A、油脂属于酯类 |
| B、油脂的氢化又叫油脂的硬化 |
| C、淀粉和纤维素的通式都是(C6H10O5)n,是同分异构体 |
| D、葡萄糖能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②③④ |
| C、①③④ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
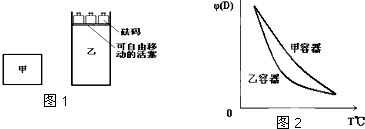
| A、甲容器中的反应先达到化学平衡状态 |
| B、两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2所示 |
| C、两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量也相同 |
| D、在甲容器中再充入2molA和2molB,平衡后甲中物质C的浓度与乙中物质C的浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液溴和苯分别受热变为气体 |
| B、干冰和氯化铵分别受热变为气体 |
| C、二氧化硅和铁分别受热熔化 |
| D、食盐和葡萄糖分别溶解在水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl和NaOH反应的中和热△H=-57.3kJ?mol-1,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ?mol-1 |
| B、CO(g)的燃烧热是283.0 kJ?mol-1,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0 kJ?mol-1 |
| C、牺牲阳极阴极保护法是应用电解原理防止金属的腐蚀 |
| D、用洁净玻璃棒蘸取某溶液点在湿润的pH试纸上,与标准比色卡对比即可测定该溶液pH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、78 | B、140 |
| C、156 | D、172 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法错误的是( )
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法错误的是( )| A、用KI淀粉试纸和食醋无法检验加碘盐中是否含有碘 |
| B、足量Cl2能使湿润的KI淀粉试纸变白的原因可能是:5Cl2+I2+6H2O→2HIO3+10HCl |
| C、由图可知氧化性的强弱顺序为Cl2>IO3->I2 |
| D、途径Ⅱ中若生成1 mol I2,反应中转移的电子数为10NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com