
(16分)实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量。测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出。(化学式量:Na2CO3-106,NaHCO3-84)
(1)分别写出上述转化反应的离子方程式:
________ _ ___、_______ ______。
(2)某天然碱的化学式为xNa2CO3·NaHCO3·2H2O,为了测定其组成,取0.3320 g样品于锥形瓶中,加适量蒸馏水使之溶解,加入几滴酚酞,用0.1000 mol·L-1的盐酸滴定至溶液由红色变无色,消耗盐酸20.00mL;再向已变无色的溶液中加入几滴甲基橙,继续用该盐酸滴定至溶液由黄色变橙色,又消耗盐酸30.00mL。
① 实验时用到的玻璃仪器有烧杯、胶头滴管、锥形瓶、____________。
② 该天然碱化学式中x=_____ ____。
(3)某学习小组在实验室中制备Na2CO3,假设产品中含有少量NaCl、NaHCO3杂质,设计实验方案进行检验,完成下表。
限选试剂:0.1000 mol·L-1盐酸、稀硝酸、AgNO3溶液、酚酞、甲基橙、蒸馏水
|
实验步骤 |
结果分析 |
|
步骤1:取少量样品于试管中,加入适量蒸馏水使之溶解,_____________________。 |
有白色沉淀生成,说明产品中含有NaCl。 |
|
步骤2:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000 mol·L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积V1。
_____________________,记录消耗盐酸的体积V2。 |
______ ______, 说明产品中含有NaHCO3。 |
(1)CO32-+H+=HCO3-(2分) HCO3-+H+=CO2↑+H2O(2分)
(2)①玻璃棒、 酸式滴定管(2分) ② 2(3分)
(3)
|
实验步骤 |
结果分析 |
|
步骤1:滴加足量稀硝酸酸化,再滴加几滴AgNO3溶液(3分) |
|
|
步骤2:再向已变无色的溶液中滴加几滴甲基橙,继续用该盐酸滴定至溶液由黄色变为橙色(2分) |
V2>V1(2分) |
【解析】(1)碳酸钠和盐酸反应是分步进行的,方程式分别是CO32-+H+=HCO3-、HCO3-+H+=CO2↑+H2O。
(2)①溶解样品还需要玻璃棒玻璃棒;滴定是还需要酸式滴定管盛放盐酸。
②两次消耗的盐酸分别是20ml和30ml,因此根据方程式可知,样品中碳酸钠和碳酸氢钠的物质的量之比是2︰1的,所以x=2。
(3)检验氯离子一般用硝酸酸化的硝酸银溶液,现象是生成氯化银白色沉淀;根据反应的方程式可知,如果含有碳酸氢钠,则第二次消耗的盐酸体积大于第一次消耗的盐酸体积,即V2>V1。


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 结果分析 |
| 步骤1:取少量样品于试管中,加入适量蒸馏水使之溶解, 滴加足量稀硝酸酸化,再滴加几滴AgNO3溶液 滴加足量稀硝酸酸化,再滴加几滴AgNO3溶液 . |
有白色沉淀生成,说明产品中含有NaCl. |
| 步骤2:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000mol?L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积V1. 再向已变无色的溶液中滴加几滴甲基橙,继续用该盐酸滴定至溶液由黄色变为橙色 再向已变无色的溶液中滴加几滴甲基橙,继续用该盐酸滴定至溶液由黄色变为橙色 ,记录消耗盐酸的体积V2. |
V2>V1 V2>V1 ,说明产品中含有NaHCO3. |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
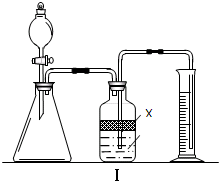 实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量.测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时,Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出.
实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量.测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时,Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出.| 实验步骤 | 结果分析 |
| 步骤①:取少量样品于试管中,加入适量蒸馏水使之溶解, |
有白色沉淀生成,说明产品中含有NaC1 |
| 步骤②:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000mol?L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积Vl; |
品中含有NaHCO3 |
查看答案和解析>>
科目:高中化学 来源:2013届广东省汕头市潮阳一中高三上学期第一次月考理综化学试卷(带解析) 题型:实验题
(16分)实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量。测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出。(化学式量:Na2CO3-106,NaHCO3-84)
(1)分别写出上述转化反应的离子方程式:
________ _ ___、_______ ______。
(2)某天然碱的化学式为xNa2CO3·NaHCO3·2H2O,为了测定其组成,取0.3320 g样品于锥形瓶中,加适量蒸馏水使之溶解,加入几滴酚酞,用0.1000 mol·L-1的盐酸滴定至溶液由红色变无色,消耗盐酸20.00mL;再向已变无色的溶液中加入几滴甲基橙,继续用该盐酸滴定至溶液由黄色变橙色,又消耗盐酸30.00mL。
①实验时用到的玻璃仪器有烧杯、胶头滴管、锥形瓶、____________。
②该天然碱化学式中x=_____ ____。
(3)某学习小组在实验室中制备Na2CO3,假设产品中含有少量NaCl、NaHCO3杂质,设计实验方案进行检验,完成下表。
限选试剂:0.1000 mol·L-1盐酸、稀硝酸、AgNO3溶液、酚酞、甲基橙、蒸馏水
| 实验步骤 | 结果分析 |
| 步骤1:取少量样品于试管中,加入适量蒸馏水使之溶解,_____________________。 | 有白色沉淀生成,说明产品中含有NaCl。 |
| 步骤2:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000 mol·L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积V1。 _____________________,记录消耗盐酸的体积V2。 | ______ ______, 说明产品中含有NaHCO3。 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量.测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时,Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出.
实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量.测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时,Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出.| 实验步骤 | 结果分析 |
| 步骤①:取少量样品于试管中,加入适量蒸馏水使之溶解, ______ | 有白色沉淀生成,说明产品中含有NaC1 |
| 步骤②:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000mol?L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积Vl;______,记录消耗盐酸的体积V2 | ______,说明产 品中含有NaHCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com