
| A. | 添加A物质 | B. | 升高体系温度 | C. | 及时分离出C物质 | D. | 减少B物质 |
科目:高中化学 来源: 题型:填空题
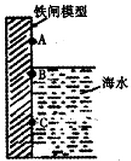 铁闸中的A、B、C三点中,C点的电极反应方程式为Fe-2e-=Fe2+将此铁闸与电源的负极相连可起到保护该铁闸的作用.对铁制品进行钝化处理可提高其抗腐蚀能力,下面是处理过程中的一个反应的方程式为:请配平该反应方程式.
铁闸中的A、B、C三点中,C点的电极反应方程式为Fe-2e-=Fe2+将此铁闸与电源的负极相连可起到保护该铁闸的作用.对铁制品进行钝化处理可提高其抗腐蚀能力,下面是处理过程中的一个反应的方程式为:请配平该反应方程式.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V1>V2>V3 | B. | V1<V2<V3 | C. | V1=V2>V3 | D. | V1=V2<V3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中C、H、O的个数比为1:2:1 | B. | 分子中C、H的个数比为1:2 | ||
| C. | 该有机物是烯烃、符合通式CnH2n | D. | 该分子中肯定不含氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇与乙酸的酯化反应 | |
| B. | 乙醇在140℃时脱水生成乙醚 | |
| C. | 乙酸乙酯的水解反应 | |
| D. | 乙醇与H2SO4、溴化钠共热制取溴乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | NaHSO3 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 5.8 | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| 序号 | Ba(OH)2溶液体积/mL | 盐酸体积/mL | 混合液pH |
| 1 | 22.00 | 0 | 10 |
| 2 | 22.00 | 18.00 | 9 |
| 3 | 22.00 | 22.00 | 8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com