
称取样品
请根据实验填写以下空白:

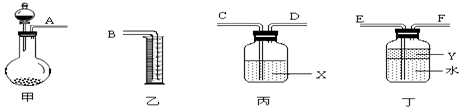
(1)若用上图所示仪器组装进行上述实验,气流从左到右,各仪器的正确连接顺序为______接 , 接 , 接 ;X溶液是 ,汽油的作用是 。
(2)操作时,怎样才能正确地测出放出气体的体积?
(3)若实验中加入硫酸溶液的体积为5.00mL,则样品中Na2SO3的质量分数是 ,一定含有的杂质是 (通过计算回答)。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022

(1)若用下图所示仪器组装进行上述实验,气流从左到右,各仪器的正确连接序为________接________,________接________,________接________;X溶液是________,汽油的作用是________。
(2)操作时,怎样才能正确地测出放出气体的体积?
(3)若实验中加入硫酸溶液的体积为5.0mL,则样品中Na2SO3的质量分数是________,一定含有的杂质是(通过计算回答)。
查看答案和解析>>
科目:高中化学 来源:2001~2002学年度第二学期形成性练习 题型:058
实验室有一瓶可能含有NaCl、![]() 、
、![]() 、
、![]() 、
、![]() 中的一种或几种杂质的
中的一种或几种杂质的![]() ,通过下列实验确定该样品的成份及
,通过下列实验确定该样品的成份及![]() 的质量分数.
的质量分数.
称取样品6.30g,加入6.0mol/L的硫酸至过量,产生无色气体560mL(标况),向逸出气体后的溶液中加入稍过量的![]() 溶液,得白色沉淀9.32g,透过蓝色钴玻璃观察,滤液的焰色反应无紫色.请根据实验填写以下空白:
溶液,得白色沉淀9.32g,透过蓝色钴玻璃观察,滤液的焰色反应无紫色.请根据实验填写以下空白:
(1)若用下图所示仪器组装进行上述实验,气流从左至右,各仪器的正确连接顺序为________接________,________接________,________接________;X溶液是________,汽油的作用是________.

(2)操作时,怎样才能正确地测出放出气体的体积?
________________________________________________________
________________________________________________________
(3)若实验中加入硫酸溶液的体积为5.00mL,则样品中![]() 的质量分数是________,一定含有的杂质是________.(通过计算回答)
的质量分数是________,一定含有的杂质是________.(通过计算回答)
查看答案和解析>>
科目:高中化学 来源: 题型:
称此样品6.30 g,加入6.0 mol·L-1的硫酸至过量,产生无色气体560 mL(标准状况),向逸出气体后的溶液中加入稍过量的BaCl2溶液,得到白色沉淀9.32 g,透过蓝色钴玻璃观察,滤液的焰色反应无紫色。请根据实验填写下列空白:
(1)若用下图所示仪器组装进行上述实验,气体从左到右各仪器的正确连接顺序为_______接_______,_______接________,______接________;X溶液是_____________,汽油的作用是___________________________________________________。

(2)操作时,怎样才能正确地测出放出气体的体积?__________________________________。
(3)若实验中加入硫酸溶液的体积为5.00 mL,则样品中Na2SO3的质量分数是多少(写出计算过程)。
(4)相关离子方程式是___________________________________________________。
(5)一定含有的杂质是什么?(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com