
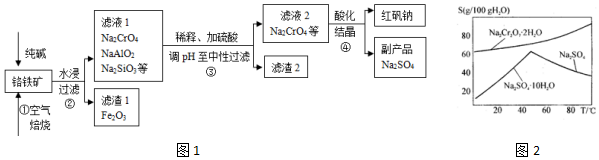
���� ��������Ҫ�ɷ�Ϊ�Ǹ�������FeCr2O4������Al2O3��SiO2�����ʣ��м��봿�ͨ�������գ������ķ�Ӧ�У�4FeCr2O4+8Na2CO3+7O2$\frac{\underline{\;����\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2��Al2O3+Na2CO3$\frac{\underline{\;����\;}}{\;}$2NaAlO2+CO2����SiO2+Na2CO3$\frac{\underline{\;����\;}}{\;}$Na2SiO3+CO2����Fe2O3������ˮ��ˮ�����˳�ȥ������Һ�м���ϡ�������pH�����ԣ�Na2SiO3��2NaAlO2���ɲ��ܵ�H2SiO3��Al��OH��3�����ˣ���������ΪH2SiO3��Al��OH��3������Һ�ữ��2CrO42-+2H+?Cr2O72-+H2O���IJ�Ʒ���ݴ˷������
��� �⣺��1��FeCr2O4����Ԫ�ػ��ϼ���+2�ۣ���Ԫ��-2�ۣ����Ԫ�ػ��ϼ�+3�ۣ������ʡ���ʯӢ�ʡ����������ж������裬��������̼���Ʒ�Ӧ����ѡ�����ʡ������������������Na2CrO4�Ļ�ѧ����ʽΪ4FeCr2O4+8Na2CO3+7O2$\frac{\underline{\;����\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2��
�ʴ�Ϊ��+3����������4FeCr2O4+8Na2CO3+7O2$\frac{\underline{\;����\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2��
��2��������У������ڻ�������Ӧ��ĽӴ������ʹ��Ӧ���ʼӿ죬�������������������״̬����Ӧ���ʽϿ죻
�ʴ�Ϊ�������ڻ�������Ӧ��ĽӴ������ʹ��Ӧ���ʼӿ죻
��3������ʱ���õ��IJ���������©�����ձ�����������
�ʴ�Ϊ��©�����ձ�����������
��4������ϡ�������pH�����ԣ�Na2SiO3��2NaAlO2���ɲ��ܵ�H2SiO3��Al��OH��3�����ˣ���������ΪH2SiO3��Al��OH��3��
�ʴ�Ϊ��H2SiO3��H4SiO4��SiO2•H2O����Al��OH��3��
��5���ữ��Ŀ����ʹCrO42-ת��ΪCr2O72-����CrO42-��������������H+���ӷ�Ӧ����Cr2O72-���÷�ӦΪ���淴Ӧ����Ӧ�����ӷ���ʽΪ2CrO42-+2H+?Cr2O72-+H2O��
�ʴ�Ϊ��2CrO42-+2H+?Cr2O72-+H2O��
��6����ͼ2��֪���¶ȸ������������ƽᾧ���������Է�ֹNa2Cr2O7•2H2O�ᾧ��������ø���ƷNa2SO4��ʵ���������Ϊ����Һ2����Ũ������ȹ��˵ø���ƷNa2SO4��
�ʴ�Ϊ������Һ2����Ũ������ȹ��˵ø���ƷNa2SO4��
���� ���⿼�黯ѧ�������̡����ʵķ����ᴿ���Բ�����������������ۡ������ݼ�ͼ��ķ����ȣ���Ŀ�ۺ��Խϴ��ض�ѧ���ۺ������Ŀ��飬����ԭ��������Ԫ�ػ����������ǹؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaAlO2��Һ��ͨ�����CO2���壺AlO2-+CO2+2H2O�TAl��OH��3��+HCO3- | |
| B�� | NH4 HCO3��Һ��������NaOH��Һ��Ӧ��HCO3-+OH-�TCO32-+H2O | |
| C�� | ��Al2��SO4��3��Һ�м��������NaOH��Һ��Al3++3OH-�TAl��OH��3�� | |
| D�� | ��FeI2��Һ��ͨ������Cl2��2Fe2++Cl2�T2Fe3++2Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʹ��̪���ɫ����Һ��NH4+��Ca2+��NO3-��Cl- | |
| B�� | c��OH-��=1��10-13mol•L-1����Һ��Na+��K-��ClO-��SO42- | |
| C�� | 0.1mol•L-1��FeCl2��Һ��K+��Na+��SO42-��Br- | |
| D�� | 0.1mol•L-1������KMnO4��Һ��Na+��Mg2+��NO3-��SO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӻ�����10�����ӵ���ԭ�ӣ�818O | |
| B�� | HF�ĵ���ʽ��H+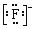 | |
| C�� | Cl-���ӵĽṹʾ��ͼ��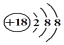 | |
| D�� | N2�Ľṹʽ����N��N�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
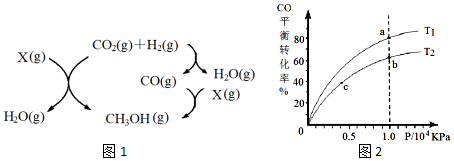
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
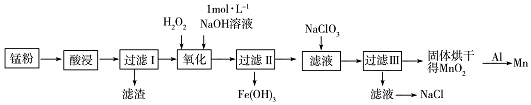
 ��NaClO3�������Ļ�ѧ�����������Ӽ����ۼ���
��NaClO3�������Ļ�ѧ�����������Ӽ����ۼ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | l04g����ϩ��C6H5-CH=CH2���к���8NA��̼�����4NA��̼̼˫�� | |
| B�� | ��50g��������Ϊ46%���Ҵ�ˮ��Һ�У�������ԭ����Ϊ3NA | |
| C�� | lmol�л���CH3-CH=CH-CH2-CH3�������9NA��ԭ����ͬһƽ���� | |
| D�� | 80��ʱ��pH=13��Ba��OH��2��Һ�к��е�OH-��ĿΪ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ܢۢ� | B�� | �ܢۢڢ� | C�� | �ڢۢܢ� | D�� | �ܢۢ٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.5molOH-�еĵ��� | B�� | 1mol H2�е�Hԭ�� | ||
| C�� | 0.6mol H2SO4�е�Oԭ�� | D�� | 1molNa��ȫ��Ӧ��ʧȥ�ĵ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com