
(12分)【化学——物质结构与性质】
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)和Fe(CO)x等。
①基态Fe3+的M层电子排布式为 ;
②尿素(H2NCONH2)分子中C原子的杂化方式是 ;
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x= 。
Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于 (填晶体类型)。
(2)下列说法正确的是 (填字母序号)。
A.第一电离能大小:S>P>Si
B.电负性顺序:C<N<O<F
C.因为晶格能CaO比KCl高,所以KCl的熔点比CaO熔点低
D.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
(3)O和Na的一种只含有离子键的化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为 。已知该晶胞的密度为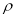 g·cm-3,阿伏加德罗常数为NA,求晶胞边长a= cm。(用含
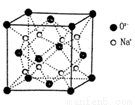
g·cm-3,阿伏加德罗常数为NA,求晶胞边长a= cm。(用含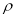 、NA的计算式表示)
、NA的计算式表示)
(1)①3s23p63d5;②sp2;③5;分子晶体。(2) BC。(3)立方体。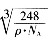 。
。
【解析】
试题分析: (1)①铁为26号元素,根据构造理论知,基态Fe3+的M层电子排布式为3s23p63d5;②尿素(H2NCONH2)分子中C与3个原子成键,碳原子的杂化方式是sp2;③铁的价电子数为8,每个配体提供一个电子对,则8+2x=18,故x=5;Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于分子晶体。(2) A.同周期元素第一电离能由左向右逐渐增大,但P元素p轨道为半充满状态,性质稳定,故第一电离能大小:P>S>Si,错误;B.同周期元素电负性由左向右逐渐增大,电负性顺序:C<N<O<F,正确;C.离子晶体熔点的高低取决于晶格能大小,因为晶格能CaO比KCl高,所以KCl的熔点比CaO熔点低,正确;D.分子晶体熔化克服分子间作用力,与共价键键能大小无关,错误,选BC。(3)由题给氧化钠的晶胞结构知,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为立方体。由题给氧化钠的晶胞结构知,1个晶胞含有Na+:8个,O2-:8×1/8+6×1/3=4个,该晶胞质量=4×62/NAg,该晶胞的密度为ρ g?cm-3,则晶胞边长a=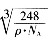 cm。
cm。
考点:考查物质结构与性质,涉及原子结构、原子间的成键方式、配合物、元素周期律及晶体结构、晶胞计算。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014山东省济宁市3月质量检测高一化学试卷(解析版) 题型:选择题
元素R有如下反应:RO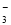 +5R-+6H+===3R2+3H2O,下列说法正确的是( )
+5R-+6H+===3R2+3H2O,下列说法正确的是( )
A.元素R位于周期表中第ⅤA族
B.RO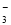 中的R只能被还原
中的R只能被还原
C.每反应消耗1 mol RO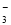 ,转移电子的物质的量为5 mol
,转移电子的物质的量为5 mol
D.R2在常温常压下一定是气体
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市高二5月月考化学试卷(解析版) 题型:选择题
某学生做乙醛还原性的实验,取l mol/L的硫酸铜溶液2 mL和0.4mol/L的氢氧化钠溶液 4 mL,在一支试管里混合后加入0.5 mL 40%的乙醛溶液加热至沸腾,无红色沉淀,实验失败的原因是( )
A.氧氧化钠的量不够 B.硫酸铜不够量
C.乙醛溶液太少 D.加热时间不够
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济南市高三5月针对性训练理综化学试卷(解析版) 题型:实验题
(12分)【化学——化学与技术】
工业上以黄铁矿为原料,采用接触法生产硫酸。请回答下列问题:
(1)煅烧黄铁矿的设备名称是__________,进料前必须将黄铁矿粉碎,目的是________。所得炉渣的用途有__________________________(填一种用途)。
(2)进入接触室前的气体必须经过净化处理,目的是防止________________________________。
(3)生产过程中,吸收三氧化硫常用的物质是_____________________________。
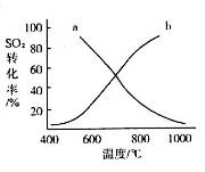
(4)温度变化与二氧化硫转化率的变化关系可用下图中的曲线______(填“a”或“b”)表示。
(5)工业上常用熟石灰和硫酸处理、回收尾气中的有害气体。反应的化学方程式为:
________________________________、_________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济南市高三5月针对性训练理综化学试卷(解析版) 题型:选择题
“神十”宇航员使用的氧气瓶是以聚酯玻璃钢为原料。甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料。下列说法中,错误的是
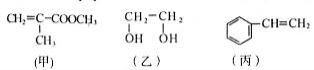
A.甲物质可以在引发剂作用下生成有机高分子化合物
B.1 mol乙物质可与2 mol钠完全反应生成1 mol氢气
C.丙物质能够使酸性高锰酸钾溶液退色
D.甲、乙、丙三种物质都可以发生加成反应
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省泰安市高三第二轮复习质量检测理综化学试卷(解析版) 题型:选择题
下列各示意图与对应的表述正确的是

A.图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应
B.图②表示在四羟基合铝酸钠溶液中加入盐酸,产生沉淀的质量变化
C.图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化
D.图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省枣庄市2013-2014学年高三3月调研考试理综化学试卷(解析版) 题型:简答题
(12分)[化学——有机化学基础]有机物A出发合成E和F,有如下转化关系。请回答:
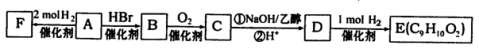
(1)已知F是一种芳香醇,分子中无甲基,则A的结构简式为 。
(2)C→D中的反应类型有 ,反应①的化学方程式为 。
(3)已知反应RCH=CHR'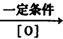 RCOOH+R'COOH,将A在此条件下反应得到两种酸X、Y,其中X为芳香族化合物,则X的结构简式为 ,名称是 。
RCOOH+R'COOH,将A在此条件下反应得到两种酸X、Y,其中X为芳香族化合物,则X的结构简式为 ,名称是 。
(4)从A到D变化中,A→B反应的目的是 。
(5)若F的同分异构体遇FeCl3溶液显紫色,核磁共振氢谱显示分子中有四种不同的氢原子,则符合此条件的F的同分异构体的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省日照市高三5月二模理综化学试卷(解析版) 题型:选择题
在2L恒容密闭容器中充入2 mol X和lmol Y发生反应:2X(g)+Y(g) 3Z(g)△H<0, 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g)△H<0, 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
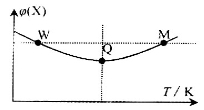
A.升高温度,平衡常数增大
B.W点X的正反应速率等于M点X的正反应速率
C.Q点时,Y的转化率最大
D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省兰陵县下学期期中考试高二化学试卷(解析版) 题型:选择题
分子式为C4H9Cl的同分异构体有( )
A.1种 B.2种 C.3种 D.4种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com