
【题目】下列说法正确的是( )
A.氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物
B.碘晶体受热转变成碘蒸气,破坏了共价键
C.CH3CH2CH2OH和CH3CH2OCH3互为同分异构体
D.加热氧化镁使之熔化克服的是共价键
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】依据叙述,写出下列反应的热化学方程式:
(1)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量。其热化学方程式为________。
(2)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650 kJ的热量。其热化学方程式为______________________________。
(3)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气(含烃类、CO、NO和SO2等)是空气的主要污染源。治理方法之一是在汽车排气管上加装“催化转化器”,使CO和NO反应产生可参与大气循环的无毒气体,促使烃类充分燃烧及SO2的转化。下列说法中错误的是( )
A. CO和NO反应生成CO2和N2反应方程式为2CO+2NO![]() 2CO2+N2
2CO2+N2
B. 汽车改用天然气为燃料或开发氢能源,都可减少对空气的污染
C. 此方法的缺点是由于CO2的增多,会大大提高空气的酸度
D. 增大绿化面积,多植树造林,可有效控制城市空气污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取50mL0.3mol/L的硫酸注入250mL容量瓶中,加水稀释至刻度线,则该溶液中的H+的物质的量浓度为
A. 0.06mol/L B. 0.12 mol/L C. 0.24mol/L D. 0.03mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C在元素周期表中的位置如图所示,已知A、B、C三种元素的原子核外电子数之和等于B的质子数的2倍。据此回答下列问题:
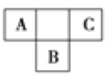
(1)A的气态氢化物的化学式为_________。
(2)B的元素符号为__________,在周期表中位于___________________。
(3)C的单质的化学式为__________,其氢化物的水溶液可用于雕刻玻璃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用如图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。

填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学方程式____________;
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象__________________。
(3)容器c中NaOH溶液的作用是____________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因。①________________________、②_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A的产量能衡量一个国家石油化工发展水平,F的碳原子数为D的两倍,以A为原料合成F,其合成路线如图所示:

(1)写出决定B、D性质的重要原子团的名称:
B________、D________。
(2)A的结构式为____________。
(3)写出下列反应的化学方程式并注明反应类型:
①______________________,反应类型:_______;
②_________________,反应类型:________。
(4)实验室怎样区分B和D?___________。
(5)除去F中少量B和D的最好试剂是________(填字母)。
A 饱和碳酸钠溶液 B 氢氧化钠溶液 C 苯 D 水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按反应N2H5++4Fe3+……→4Fe2++Y+……,在水溶液中N2H5+离子将Fe3+还原为Fe2+,作为N2H5+离子的氧化产物Y可能为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com