
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
20℃时,NaCl溶解于水的实验数据如下表所
| 实验序号 | 加入水的质量/g | NaCl质量/g | 未溶的NaCl质量/g |
| ① | 10 | 4 | 2 |
| ② | 20 | 4 | 0 |
| ③ | 30 | 4 | 0 |
A.实验①所得溶液为饱和溶液 B.实验②所得溶液为饱和溶液
C.20℃时NaCl的溶解度为2g D.实验③所得溶液的溶质质量分数为13.3%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列方法中,正确的是
A.用湿润的红色石蕊试纸检验氨气
B.在样品溶液中先加入硝酸银溶液,再加入稀硝酸,若白色沉淀存在,则样品中含有Cl—
C.将熟石灰和氯化铵混合加热,可以制备氨气
D.将烧瓶中的浓氨水加热
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.用金属钠可区分乙醇和乙醚 B.用高锰酸钾酸性溶液可区分己烷和3-己烯
C.用水可区分苯和溴苯 D.用新制的银氨溶液可区分甲酸甲酯和乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
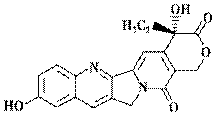
具有显著抗癌活性的10羟基喜树碱的结构如图所示。
下列关于10羟基喜树碱的说法正确的是
A. 分子式为C20H16N2O5
B. 不能与FeCl3溶液发生显色反应
C. 不能发生酯化反应
 D. 一定条件下,1 mol该物质最多可与1 mol NaOH反应
D. 一定条件下,1 mol该物质最多可与1 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
乙醇是重要的有机化工原料,可由乙烯气相直接水合法间接水合法生产,回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),再水解生成乙醇,写出相应反应的化学方程式__________________________________。
(2)已知:
甲醇脱水反应 2CH3OH(g)=CH3OCH3(g)+H2O(g) △H=-23.9kJ/mol
甲醇制烯烃反应 2CH3OH(g)=C2H4(g)+2H2O(g) △H=-29.1kJ/mol
乙醇异构化反应 C2H5OH(g)=CH3OCH3(g) △H=+50.7kJ/mol
则乙烯气相直接水合反应C2H4(g)+2H2O(g)= C2H5OH(g)的△H=________kJ/mol,与间接水合法相比,气相直接水合法的优点是___________________________。
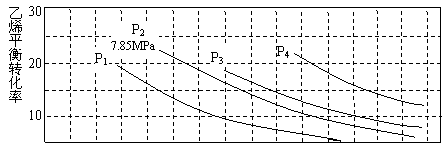
(3)下图为气相水合法中乙烯的平衡转化率与温度、压强的关系(n(H2O):n(C2H4)=1:1)。
 |
|
①列算式计算乙烯水合制乙醇反应在图中A点的平衡常数Kp=_______________
_____________。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
②图中压强(P1、P2、P3、P4)的大小顺序为___________,理由是_________________。
③气相直接水合法常采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290℃、
压强6.9MPa,n(H2O):n(C2H4)=0.6:1。乙烯的转化率为5%,若要进一步提高乙烯转化率,除了可以适当改变温度和压强外,还可以采取的措施有___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com