
如图所示,气体a的主要成分是氯气,杂质是空气和水蒸气,回答下列问题:
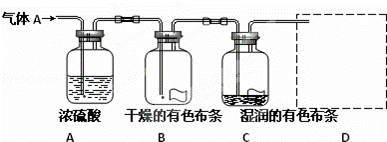
(1)该实验的现象是 .
(2)由以上现象得到的结论是 .
(3)该设计还存在事故隐患,请在D处虚线方框内画出处理事故隐患的措施图形(画在答题纸上)并标明所用试剂,处理过程中的离子方程式为
(4)若没有A装置,可能出现的现象是 ,结合方程式说明出现这种现象的原因是 .
考点: 探究氯水、氯气的漂白作用.
分析: (1)干燥的氯气通入B,不能使干燥的有色布条褪色,在通入湿润的有色布条,布条褪色,证明干燥氯气不具有漂白性,次氯酸具有漂白性;
(2)干燥氯气不具有漂白性,氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性;
(3)氯气有毒,必须进行尾气处理,可用NaOH溶液进行尾气处理,防止其造成空气污染,氯气和氢氧化钠反应生成氯化钠、次氯酸钠、和水;
(4)若没有A装置,气体中有水,可能两布条都褪色;氯气与水反应生成次氯酸.
解答: 解:(1)干燥的氯气通入B,不能使干燥的有色布条褪色,在通入湿润的有色布条,布条褪色,证明干燥氯气不具有漂白性,次氯酸具有漂白性,故答案为:干燥的有色布条不褪色,而湿润的有色布条褪色;
(2)干燥氯气不具有漂白性,氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,故答案为:氯气无漂白性,次氯酸有漂白性;
(3)氯气有毒,必须进行尾气处理,可用NaOH溶液进行尾气处理,防止其造成空气污染,氯气和氢氧化钠反应生成氯化钠、次氯酸钠、和水,所以处理过程中的离子方程式为Cl2+2OH﹣=Cl﹣+ClO﹣+H20,装置图为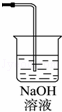 ;
;
故答案为: ;Cl2+2OH﹣=Cl﹣+ClO﹣+H20;
;Cl2+2OH﹣=Cl﹣+ClO﹣+H20;
(4)若没有A装置,气体中有水,可能两布条都褪色;氯气与水反应生成次氯酸,方程式为:Cl2+H20⇌Cl﹣+HClO+H+,故答案为:可能两布条都褪色;水蒸气与氯气反应,Cl2+H20⇌Cl﹣+HClO+H+,生成的次氯酸有漂白性.
点评: 本题考查氯气的性质,氯水微粒的性质,需要注意的是氯气没有漂白性,氯水的漂白性是溶液中次氯酸的表现的性质.


科目:高中化学 来源: 题型:
配制一定体积、一定物质的量浓度的溶液时,下列会使配得的溶液浓度偏低的是()
A. 容量瓶中原有少量蒸馏水
B. 溶液从烧杯转移到容量瓶中后没有洗涤烧杯和玻璃棒
C. 定容时观察液面俯视
D. 定容时平视液面
查看答案和解析>>
科目:高中化学 来源: 题型:
某食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:
①加入稍过量的Na2CO3溶液;
②加入稍过量的NaOH溶液;
③加入稍过量的BaCl2溶液;
④滴入稀盐酸至无气泡产生;
⑤过滤;
正确的操作顺序是()
A. ③②①⑤④ B. ①②③⑤④ C. ②③①⑤④ D. ③⑤②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在无色透明的酸性溶液中能大量共存的是()
A. Fe3+、HCO3﹣、Cl﹣、Na+ B. SO42﹣、NO3﹣、Ba2+、Cu2+
C. MnO4﹣、Na+、K+、Mg2+ D. Ca2+、Cl﹣、NO3﹣、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
关于胶体的下列叙述中正确的是()
A. 胶体和溶液、浊液的本质区别是胶体有丁达尔效应
B. 实验室制取氢氧化铁胶体的反应是复分解反应
C. 浊液中的粒子不能透过半透膜,胶体和溶液中的粒子则能透过
D. 胶体都是无色透明的液体
查看答案和解析>>
科目:高中化学 来源: 题型:
如果Mg2﹣、NO3﹣、Na﹣和M四种离子以物质的量之比为1:2:4:2共同存在同一种溶液中,那么M可能是()
A. K+ B. Cl﹣ C. CO32﹣ D. SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
下列四类反应:①置换反应 ②复分解反应 ③没有单质参加的化合反应 ④只有一种元素化合价发生变化的反应 ⑤离子反应,其中一定不是氧化还原反应的是()
A. 只有② B. 只有②③ C. 只有③④ D. ①②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com