
|
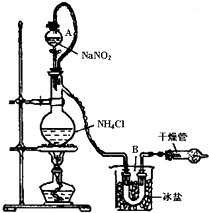
�ڻ�������г��ü����ܷ����ⶨ������S02�ĺ�����ԭ����S02��KIO3������Ӧ����һ���л�����ָʾ��������ܷ�Ӧ����(δ��ƽ)�� ��KIO3��SO2��H2O��I2��H2SO4��KHSO4����KIO3��SO2��H2O��KI��H2SO4 ������˵����ȷ���� | |
| [����] | |
A�� |
�����ܷ��ǰ��շ�Ӧ��ԭ����Ƶ� |
B�� |
�����ܷ��ǰ��շ�Ӧ��ԭ����Ƶ� |
C�� |
��Ӧ�٢ھ�������Ƴɼ����ܷ��������ǵ���ͬ��KIO3������SO2�٣����Լ����ܷ��ǰ�����Ƶ� |
D�� |
��Ӧ�٢ھ�������Ƴɼ����ܷ��������ǵ���ͬ��KIO3������SO2�࣬���Լ����ܷ��ǰ�����Ƶ� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �Ȼ����һ����Ҫ�Ļ���ԭ�ϣ�Ӧ�ù㷺��
�Ȼ����һ����Ҫ�Ļ���ԭ�ϣ�Ӧ�ù㷺��
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��KIO3+SO2+H2O![]() I2+H2SO4+KHSO4
I2+H2SO4+KHSO4
��KIO3+SO2+H2O![]() KI+H2SO4
KI+H2SO4
������˵����ȷ����
A.�����ܷ��ǰ��շ�Ӧ��ԭ����Ƶ�
B.�����ܷ��ǰ��շ�Ӧ��ԭ����Ƶ�
C.��Ӧ�٢ھ�������Ƴɼ����ܷ��������ǵ���ͬ��KIO3������SO2�٣����Լ����ܷ��ǰ�����Ƶ�
D.��Ӧ�٢ھ�������Ƴɼ����ܷ��������ǵ���ͬ��KIO3������SO2�࣬���Լ����ܷ��ǰ�����Ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��KIO3+SO2+H2O��I2+H2SO4+KHSO4 ��KIO3+SO2+H2O��KI+H2SO4������˵����ȷ����( )
A.�����ܷ��ǰ��շ�Ӧ��ԭ����Ƶ�
B.�����ܷ��ǰ��շ�Ӧ��ԭ����Ƶ�
C.��Ӧ�٢ھ�������Ƴɼ����ܷ��������ǵ���ͬ��KIO3������SO2�٣����Լ����ܷ��ǰ�����Ƶ�
D.��Ӧ�٢ھ�������Ƴɼ����ܷ��������ǵ���ͬ��KIO3������SO2�࣬���Լ����ܷ��ǰ�����Ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
��ѧ�ڻ��������Խ��Խ��ʾ����Ҫ���ã�ˮ���ܻ�ԭ�����ʣ���Ҫ���л����Ⱦ�ij̶ȳ��û�ѧ��������COD����������COD��ָ��һ�������£���ǿ����������һ�����ˮ��ʱ�����ĵ�ǿ�������൱����������������λ��mg/L��ʾ��
�ظ���ط���ָ��ǿ������Һ�У���һ�������ظ������������Ag+��������ˮ���еĻ�ԭ�����ʣ��䱾������ԭΪCr3+���������ظ����������������ָʾ�����������������Һ�صΣ���������Լ��������������ˮ���Ļ�ѧ��������COD����
��ش��������⣺
��1����ˮ���к���Ũ�Ƚϸߵ�Cl��ʱ���������HgSO4��Һ����HgSO4�����ü�����ԭ���� ��
��2���ζ�ʱ�����������Һ��ʢ���� ����ᡱ���ʽ�ζ����С�
��3�����ҡ���������ˮ�����鷨��GB5750-85�����з���ļ������Ϊ0.002 mg��L��ijˮԴ�ܻ�������Ⱦ���Ӻ�����0.282 mg/L������Ⱦ��ˮ���зӣ��Ա���������CO2���㣩����Ļ�ѧ��������COD��Ϊ mg/L��
��4��ij��������������ҵ�ŷų��ķ�ˮ�У�ij��COD����ֵ�ߴ�2100 mg/L����������ҵ���п����� ��������ĸ��
a�����dz� b��ˮ�೧ c����Ƴ� d����ֽ��
��5������ij��ˮ��Ʒ10.00 mL���ȼ���10 mL����ˮ��Ȼ�����10.00 mL 0.04000 mol/L K2Cr2O7��Һ��3 mL 1%����-��������Һ��17 mL���ṯ��Һ�����ȷ�Ӧ2 h������������ָʾ����������0.1000 mol/L Fe(NH4)2(SO4)2��Һ�ζ������K2Cr2O7������ȥFe(NH4)2(SO4)2��Һ12.00 mL���Լ����ˮ���Ļ�ѧ��������COD����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com