
【题目】在体积均为0.5L、pH均等于1的盐酸、醋酸溶液中,分别投入1.4g铁粉,则下图所示曲线比较符合客观事实的是( )
A.  B.
B. 
C.  D.
D. 
【答案】B
【解析】
铁的物质的量=![]() =0.025mol,盐酸是强酸,所以体积均为0.5L,pH均等于1的盐酸中HCl的物质的量=0.1mol/L×0.5L=0.05mol,Fe+2H+═Fe2++H2↑,根据铁和盐酸反应的关系式知,二者恰好反应;
=0.025mol,盐酸是强酸,所以体积均为0.5L,pH均等于1的盐酸中HCl的物质的量=0.1mol/L×0.5L=0.05mol,Fe+2H+═Fe2++H2↑,根据铁和盐酸反应的关系式知,二者恰好反应;
醋酸是弱酸,等pH的盐酸和醋酸,醋酸的浓度大于盐酸,所以体积均为0.5L、pH均等于1的盐酸和醋酸溶液中,醋酸的物质的量大于盐酸,所以醋酸有剩余,完全反应后,醋酸中pH小于盐酸;
盐酸恰好反应,醋酸有剩余,则生成氢气的量与铁成正比,铁的量相同,则生成的氢气的体积相同,但反应过程中,醋酸能电离出氢离子,导致醋酸溶液中氢离子浓度始终大于盐酸,则醋酸的反应速率大于盐酸,完全反应时,醋酸用的时间小于盐酸,
A、两者产生氢气的体积一样多,且醋酸的反应速率快,用时短,选项A错误;
B、与盐酸完全反应,溶液呈中性,与醋酸反应后醋酸过量,溶液呈酸性,且与醋酸反应的速率快,用时短,选项B正确;
C、醋酸中氢离子浓度保持较大,反应速率较快,用时短,选项C错误;
D、醋酸的浓度大于盐酸,反应过程中氢离子浓度大于盐酸,反应快,用时短,选项D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. NaCl(aq) ![]() Cl2
Cl2![]() 漂白粉
漂白粉
B. (C6H10O5)n(淀粉) ![]() C6H12O6(葡萄糖)
C6H12O6(葡萄糖) ![]() C2H5OH
C2H5OH
C. NH3·H2O![]() (NH4)2SO3
(NH4)2SO3![]() (NH4)2SO4
(NH4)2SO4
D. Fe2O3(s) 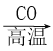 Fe(s)
Fe(s) ![]() FeCl3(aq)
FeCl3(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应的实验,能达到实验目的是

A. 实验室用甲装置制取氯气
B. 盛有水的乙装置,吸收NH3气体
C. 用丙装置对生成的气体体积进行测量可以减少误差
D. 用丁装置灼烧FeSO47H2O晶体得到固体FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:N2O4(g)![]() 2NO2(g) △H>0,平衡体系中气体的平均摩尔质量(
2NO2(g) △H>0,平衡体系中气体的平均摩尔质量(![]() )在不同温度下随压强的变化曲线如图所示。下列说法正确的是
)在不同温度下随压强的变化曲线如图所示。下列说法正确的是

A. 温度:T1<T2 B. 平衡常数:K(a)=K(b)<K(c)
C. 反应速率:v(b)>v(a) D. 当![]() =69g/mol时,n(NO2):n(N2O4)=2:1
=69g/mol时,n(NO2):n(N2O4)=2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明:丰富的CO2可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)枯竭危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环。
(1)目前工业上有一种方法是用CO2加氢合成低碳烯烃。现以合成乙烯(C2H4)为例、该过程分两步进行:
第一步:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H =+41.3kJ·mol-1
CO(g)+H2O(g) △H =+41.3kJ·mol-1
第二步:2CO(g)+4H2(g)![]() C2H4(g)+2H2O(g) △H =-210.5kJ·mol-1
C2H4(g)+2H2O(g) △H =-210.5kJ·mol-1
①CO2加氢合成乙烯的热化学方程式为_____________________________。
②一定条件下的密闭容器中,上述反应达到平衡后,要加快反应速率并提高CO2的转化率,可以采取的措施是______(填字母)。
A.减小压强 B.增大H2浓度 C.加入适当催化剂 D.分离出水蒸气
(2)另一种方法是将CO2和H2在230℃催化剂条件下生成甲醇蒸气和水蒸气。现在10L恒容密闭容器中投入1molCO2和2.75molH2,发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。在不同条件下测得平衡时甲醇的物质的量随温度、压强的变化如图所示:
CH3OH(g)+H2O(g)。在不同条件下测得平衡时甲醇的物质的量随温度、压强的变化如图所示:

①能判断该反应达到化学平衡状态的是_______(填字母)。
a.c(H2):c(CH3OH)=3:1 b.容器内氢气的体积分数不再改变
C.容器内气体的密度不再改变 d.容器内压强不再改变
②上述反应的△H______0(填“>”或“<”),图中压强p1____p2(填“>”或“<”)。
③经测定知Q点时容器的压强是反应前压强的9/10,则Q点H2的转化率为____________。
④N点时,该反应的平衡常数K=______(计算结果保留两位小数)。
(3)用生石灰吸收CO2可生成难溶电解质CaCO3,其溶度积常数Ksp=2.8×10-9。现有一物质的量浓度为2×10-4mol/L纯碱溶液,将其与等体积的CaCl2溶液混合,则生成沉淀所需CaCl2溶液的最小浓度为___mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100℃时,将0.2molN2O4(g)充入2L的恒容密闭容器中,间隔一定时间后对该容器内各物质的物质的量进行测定,得到如下数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
N(N2O4)/mol | 0.20 | n1 | 0.10 | n3 | n4 |
N(NO2)/mol | 0.00 | 0.12 | n2 | 0.24 | 0.24 |
(1)该反应的平衡常数表达式为___________________________,由表中数据分析可得,n1=____mol,n3=________________mol;
(2)在上述条件下,从0到40s内NO2的平均反应速率为___________________;
(3)该反应达到化学平衡后,下列改变可使N2O4浓度增大的是_____(填序号);
A.增大容器的容积 B.向容器中充入一定量的NO2
C.向容器中再充入一定量的N2O4 D.向容器中充入一定量的He(g)
(4)在下图中画出此反应中N2O4的浓度随时间变化的曲线_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如下图所示;

回答下列问题:
(1)A的结构简式为_____________________。
(2)由乙醇生产C的化学反应类型为_____________________。
(3)E是一种常见的塑料,其化学名称是_____________________。
(4)由乙醇生成F的化学方程式为__________________________________。
(5)写出A生成B的化学方程式____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物6.4g在氧气中完全燃烧,只生成8.8g CO2和7.2 g H2O。下列说法正确的是
A. 该化合物仅含碳、氢两种元素 B. 该化合物中碳、氢原子个数比为1:4
C. 无法确定该化合物是否含有氧元素 D. 该化合物一定是C2H8O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com