
1L 0.1mol•L﹣1的K2SO4溶液中( )
|
| A. | K+的物质的量为0.1mol |
|
| B. | SO42﹣的物质的量为0.2mol |
|
| C. | K+的物质的量浓度为0.1mol.L﹣1 |
|
| D. | SO42﹣的物质的量浓度为0.1mol.L﹣1 |
考点:
物质的量浓度的相关计算.
专题:
物质的量浓度和溶解度专题.
分析:
由化学式K2SO4可知,溶液中c(K+)=2c(K2SO4),c(SO42﹣)=c(K2SO4),根据n=cV计算离子的物质的量.
解答:
解:A、1L0.1mol/L的K2SO4溶液中,c(K+)=2c(K2SO4)=0.2mol/L,故n(K+)=1L×0.2mol/L=0.2mol,故A错误;
B、1L0.1mol/L的K2SO4溶液中,c(SO42﹣)=c(K2SO4)=0.1mol/L,故n(SO42﹣)=1L×0.1mol/L=0.1mol,故B错误;
C、0.1mol/L的K2SO4溶液中,c(K+)=2c(K2SO4)=0.2mol/L,故C错误;
D、0.1mol/L的K2SO4溶液中,c(SO42﹣)=c(K2SO4)=0.1mol/L,故D正确;
故选D.
点评:
本题考查物质的量浓度的有关计算,比较基础,注意电解质溶液中离子的浓度与电解质浓度关系,离子浓度=电解质的浓度×电解质电离出离子数目,与溶液体积无关.


科目:高中化学 来源: 题型:
在一定条件下,向某密闭容器中投入一定量的氮气和氢气,发生反应N2(g)+3H2(g)⇌2NH3(g).下列关于从反应开始至达到化学平衡的过程中正、逆反应速率变化情况的图象中,正确的是()
A. 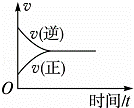 B.
B. 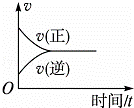 C.
C. 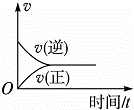 D.
D. 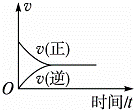
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y均为短周期主族元素,X原子的最外层有2个电子,Y原子的最外层有6个电子,这两种元素形成的常见化合物的化学式为( )
|
| A. | XY | B. | XY2 | C. | X2Y | D. | X2Y3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,2L密闭容器内,反应2NO(g)+O2(g)⇌2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
该反应达到平衡状态的时间是( )
|
| A. | 3min | B. | 1min | C. | 2min | D. | 0min |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
|
| A. | 大米富含淀粉 |
|
| B. | 加碘食盐含有碘酸钾(KIO3) |
|
| C. | 人体必需的微量元素就是维生素 |
|
| D. | 人体必需的微量元素不都是金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中,正确的是( )
|
| A. | 为使过滤速率加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动 |
|
| B. | 用酒精灯给试管加热时,要将被加热的试管放在酒精灯火焰的外焰上 |
|
| C. | 为加速固体物质的溶解只能采用加热的方法 |
|
| D. | 为增大气体物质的溶解度,常采取搅拌、加热等措施 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:Ksp(AgCl)=1.8×10﹣10,Ksp(AgI)=1.5×10﹣16,Ksp(Ag2CrO4)=2.0×10﹣12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
|
| A. | AgCl>AgI>Ag2CrO4 | B. | AgCl>Ag2CrO4>AgI |
|
| C. | Ag2CrO4>AgCl>AgI | D. | Ag2CrO4>AgI>AgCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推断正确的是()
A. SiO2是酸性氧化物,能与NaOH溶液反应
B. Na2O、Na2O2组成元素相同,与CO2反应产物也相同
C. CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
D. 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com