
分析 令烃的组成为CxHy,由燃烧通式:CxHy+(x+$\frac{y}{4}$)O2$\frac{\underline{\;点燃\;}}{\;}$xCO2+$\frac{y}{2}$H2O,可知1molCxHy消耗氧气(x+$\frac{y}{4}$)mol;
根据H原子守恒可知,分子含有H原子数目越小,生成的水越小;
根据碳原子守恒可知,生成二氧化碳的量相等.
解答 解:令烃的组成为CxHy,由燃烧通式:CxHy+(x+$\frac{y}{4}$)O2$\frac{\underline{\;点燃\;}}{\;}$xCO2+$\frac{y}{2}$H2O,可知1molCxHy消耗氧气(x+$\frac{y}{4}$)mol,烃的物质的量相等,分子中均含有2个C原子,故分子中H原子数目越大消耗氧气越多,则乙烷消耗氧气最多,结构简式为CH3CH3,乙炔分子含有H原子数目越小,根据H原子守恒乙炔生成的水越小,其结构简式为HC≡CH,根据碳原子守恒可知,生成二氧化碳的量相等,
故答案为:CH3CH3;HC≡CH;CO2.
点评 本题考查烃燃烧有关规律,注意利用燃烧通式进行解答,若烃的质量相等,H元素质量分数越大耗氧量越大,耗氧量相等时烃的最简式相同.


科目:高中化学 来源: 题型:选择题
| A. | 在铜锌原电池中,铜作负极 | |
| B. | 在铜锌原电池中,锌作阴极 | |
| C. | 原电池是将化学能转化为电能的装置 | |
| D. | 原电池是将电能转化为化学能的装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
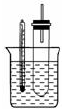 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ | |
| B. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 | |
| C. | 上述现象说明[Cu(NH3)4]2+不如Cu(OH)2稳定 | |
| D. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 现象 | 结论 |
| A | 将乙醇和苯配成相同物质的量浓度的水溶液 | 加入大小相同的金属钠,观察反应快慢 | 两者的羟基活性不同 |
| B | 向Na2SiO3溶液中通入CO2气体 | 溶液变浑浊 | 碳的非金属性比硅强 |
| C | 将过量的铁粉和氯气反应,将反应后的固体溶于盐酸后,滴加KSCN溶液 | 溶液不显红色 | 过量铁与氯气反应产物为FeCl2 |
| D | 向Al(SO4)3溶液中滴入氨水至过量 | 溶液先变浑浊后又澄清 | Al(SO4)3溶液既有酸性又有碱性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
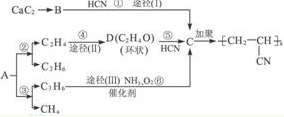 人造羊毛的主要成分为聚丙烯腈
人造羊毛的主要成分为聚丙烯腈 ,此物质可由以下三种途径合成,已知A是石油分馏的一种产品.
,此物质可由以下三种途径合成,已知A是石油分馏的一种产品.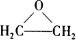 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室以2一丁醇(
实验室以2一丁醇( )为原料制备2-氯丁烷
)为原料制备2-氯丁烷 ),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:
),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:| 物质 | 熔点 (℃) | 沸点(℃) |
| 2-丁醇 | -114.7 | 99.5 |
| 2-氯乙烷 | -131.3 | 68.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com