
已知3375As、3579Br位于同一周期.下列关系正确的是()
A. 原子半径:As>Cl>P B. 热稳定性:HCl>AsH3>HBr
C. 还原性:As3﹣>S2﹣>Cl﹣ D. 酸性:H3AsO4>H2SO4>H3PO4
考点: 同一周期内元素性质的递变规律与原子结构的关系;元素周期律的作用.
专题: 元素周期律与元素周期表专题.
分析: As、Br属于同一周期元素,As位于第VA族、Br位于第VIIA族,
A.电子层数越多,其原子半径越大,同一周期元素原子半径随着原子序数增大而减小;
B.元素的非金属性越强,其气态氢化物的稳定性越强;
C.元素的非金属性越强,其简单阴离子的还原性越弱;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强.
解答: 解:As、Br属于同一周期元素,As位于第VA族、Br位于第VIIA族,
A.电子层数越多,其原子半径越大,同一周期元素原子半径随着原子序数增大而减小,所以原子半径As>P>Cl,故A错误;
B.元素的非金属性越强,其气态氢化物的稳定性越强,非金属性Cl>Br>As,所以气态氢化物的稳定性HCl>HBr>AsH3,故B错误;
C.元素的非金属性越强,其简单阴离子的还原性越弱,非金属性Cl>S>As,则简单阴离子的还原性As3﹣>S2﹣>Cl﹣,故C正确;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性S>P>As,所以酸性:H2SO4>H3PO4>H3AsO4,故D错误;
故选C.
点评: 本题考查同一周期、同一主族元素性质递变规律,明确元素非金属性与其简单阴离子的还原性、最高价氧化物的水化物酸性、气态氢化物的稳定性之间关系即可解答,题目难度不大.


科目:高中化学 来源: 题型:
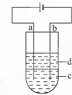
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.应用如下图所示电解实验可制得白色纯净的Fe(OH)2沉淀.两电极的材料分别为石墨和铁.
(1)a电极材料应为 ,电极反应式 ;
(2)电解液c可以是(填编号)
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用为 ,在加入苯之前对c应作怎样的简单处理? .
(4)为了在较短时间内看到白色沉淀,可采取的措施(填编号)
A.改用稀硫酸作电解液
B.适当增大电源的电压
C.适当减少两电极间距离
D.适当降低电解液的温度
(5)若c为Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一明显现象为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是()
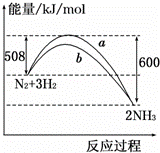
A. 该反应的热化学方程式为:N2+3H2⇌2NH3△H=﹣92 kJ/mol
B. a曲线是加入催化剂时的能量变化曲线
C. 加入催化剂,该化学反应的反应热改变
D. 在温度、体积一定的条件下,若通入2 mol N2和6 mol H2反应后放出的热量为Q kJ,则184>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,浓度都为1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z.反应2min后,测得 X2的浓度为0.4mol/L,用Y2的变化表示的反应速率v(Y2)=0.1mol/(L•min),生成的c(Z)=0.4mol/L,如z用X、Y表示,则该反应方程式是()
A. X2+2Y2═2XY2 B. 2X2+Y2═2X2Y C. 3X2+Y2═2X3Y D. X2+3Y2═2XY3
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某可逆反应m A(g)+n B(气)⇌p C(气)+Q,在密闭容器中进行,右图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线.由曲线分析,下列判断正确的是()
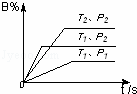
A. T1<T2,P1>P2,m+n>p,Q>0 B. T1>T2,P1<P2,m+n>p,Q<0
C. T1<T2,P1>P2,m+n<p,Q>0 D. T1>T2,P1<P2,m+n<p,Q>0
查看答案和解析>>
科目:高中化学 来源: 题型:
2﹣丁炔与1,3﹣丁二烯分别跟氢气反应的热化学方程式如下:
CH3﹣C≡C﹣CH3(g)+2H2(g)→CH3CH2CH2CH3(g)+Q1
CH2=CH﹣CH=CH2(g)+2H2(g)→CH3CH2CH2CH3(g)+Q2
已知:Q1>Q2(Q1和Q2均大于零),由此不能判断()
A. 2﹣丁炔与1,3﹣丁二烯稳定性的相对大小
B. 2﹣丁炔与1,3﹣丁二烯分子储存能量的相对高低
C. 2﹣丁炔与1,3﹣丁二烯相互转化的热效应
D. 一个碳碳叁键的键能与两个碳碳双键的键能之和的大小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 在101kPa下,1g物质完全燃烧所放出的热量叫该物质的热值,单位为kJ•mol﹣1 |
|
| B. | 某放热反应在其它条件不变时,加入催化剂后反应放出的热量会减少 |
|
| C. | 一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的 |
|
| D. | 若一个反应的焓变△H=a kJ•mol﹣1,则其逆反应△H= |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是( )

|
| A. | 蒸馏、蒸发、萃取、过滤 | B. | 蒸馏、过滤、萃取、蒸发 |
|
| C. | 萃取、过滤、蒸馏、蒸发 | D. | 过滤、蒸发、萃取、蒸馏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com