
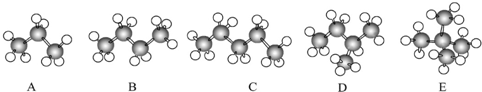
分析 (1)三者的关系为碳原子数不同的烷烃判断;CDE三者的关系是分子式相同,结构不同;
(2)丁烷有2种同分异构体,铵习惯命名法分别命名为正丁烷和异丁烷;
(3)分子中有几种不同化学环境的H原子,就有几种一氯代物,据此解答即可.
解答 解:(1)ABE三者结构相似,分子组成上相差1个或多个CH2原子团,属于同系物;CDE三者分子式相同,结构不同,属于同分异构体,故答案为:同系物;同分异构体;
(2)丁烷有2种同分异构体,分别为正丁烷和异丁烷,其中D带有一个支链,属于异丁烷,故答案为:异丁烷;
(3)E为新戊烷,其中四个甲基上的12个H是等同的,故只有1种一氯代物,结构简式为:CH2ClC(CH3)3,故答案为:1;CH2ClC(CH3)3.
点评 本题考查了烷烃及其命名、同分异构体等知识,题目难度中等,充分考查了学生的分析、理解能力和灵活应用所学知识的能力.


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某小组用如图所示装置对Cl2与Na2S2O3的反应进行探究(气密性已检验).
某小组用如图所示装置对Cl2与Na2S2O3的反应进行探究(气密性已检验).| 操作 | 现象 |
| 打开分液漏斗活塞,滴加一定量浓盐酸,加热 | i.A中有黄绿色气体生成,C中液面上方有白雾,溶液中开始出现少量浑浊; ii.一段时间后,C中产生大量黄色沉淀. |
| 用湿润的淀粉碘化钾试纸检验C中白雾 | 淀粉碘化钾试纸变蓝 |
| C中浊液过滤后,取少量滤液用盐酸酸化,滴加氯化钡溶液 | 有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含的质子数=A-n | B. | 所含电子数=Z+n | ||
| C. | 所含的中子数=A-Z | D. | 质量数=Z+A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种离子都具有相同的电子层结构 | |
| B. | 原子半径:r(D)>r(C)>r(A)>r(B) | |
| C. | 离子半径:r(B+)>r(A2+)>r(C3-)>r(D-) | |
| D. | B、D两元素的最高价氧化物的水化物在溶液中反应的离子方程式可表示为H++OH-=H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com