
【题目】下列说法不正确的是
A.2H和3H互为同位素B.O2和O3互为同素异形体
C.CH3CH2OH 和CH3OCH3互为同分异构体D.C2H2和C6H6互为同系物
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
【题目】(1)标准状况下,22.4LHCl气体溶于水,制成250mL溶液,所得溶液中氯化氢物质的量浓度为_____;若将该盐酸再稀释成1L溶液A,则其氯化氢的物质的量浓度变为_________;
(2)从A溶液取出250mL盐酸与足量Zn反应,在标准状况下可生成多少体积的气体?(根据化学方程式计算)___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种高分子化合物,常用作有机合成的中间体,并可用作乳胶漆等。可以通过以下途径合成:
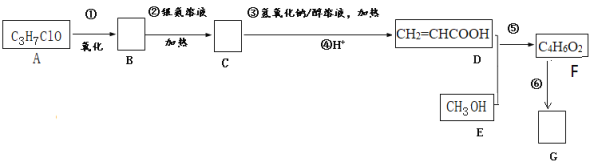
已知有机物A中含有C、H、O、Cl四种元素且同一个碳原子上不直接连接两个官能团。
(1)A的结构简式为___________或___________;反应③的反应类型_____________________。
(2) 写出反应⑤和反应⑥的化学方程式:反应⑤___________;反应⑥(在一定条件下)___________。
(3)写出1种E的同系物的名称_____________________。写出1种与F含有相同官能团的F的同分异构体的结构简式_______________。
(4)试设计一条以![]() 为原料合成
为原料合成![]() 的合成路线__________________。(合成路线常用的表示方式为:甲
的合成路线__________________。(合成路线常用的表示方式为:甲![]() 乙……
乙……![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验过程的评价,正确的是( )
A.某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐
B.某溶液中滴加BaCl2溶液,生成白色沉淀,证明一定含有SO![]()
C.某无色溶液滴入紫色石蕊试液显红色,该溶液一定显碱性
D.验证某溶液中是否含有Cl-,先加稀硝酸酸化,再加入AgNO3溶液,有白色沉淀,证明含Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在其他条件不变时,只改变某一条件,化学反应aA(g)+B(g)![]() cC(g)的平衡的变化图象如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是
cC(g)的平衡的变化图象如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是

A. 在图象反应Ⅰ中,说明正反应为吸热反应
B. 在图象反应Ⅰ中,若p1>p2,则此反应的ΔS>0
C. 在图象反应Ⅱ中,说明该正反应为吸热反应
D. 在图象反应Ⅲ中,若T1>T2,则该反应能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)等质量的氧气和臭氧其物质的量之比为___,原子个数之比为__。
(2)标准状况下,36.5gHCl气体的体积约为___。将该气体溶于水中得到2L溶液,则该溶液的浓度为____。
(3)质量分数为w的MgCl2溶液,密度为dg/mL,该溶液中氯离子的物质的量浓度为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,取0.1mol·L-1HY溶液与0.1mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=9,则下列说法正确的是
A. 混合溶液中由水电离出的c(OH-)=1×10-9mol/L
B. 混合溶液中离子浓度由大到小的顺序为c(Y-)﹥c(Na+)﹥c(OH-)﹥c(H+)
C. 混合溶液中c(OH-)-c(HY)= c(H+)=1×10-9mol/L
D. 混合溶液中c(Na+)=c(Y-)+c(HY)=0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是几种有机化合物的转换关系:
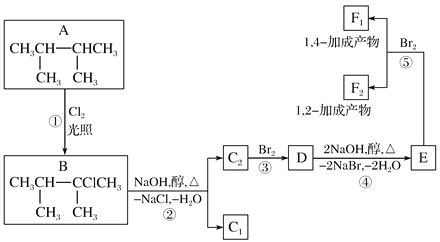
请回答下列问题:
(1)根据系统命名法,化合物A的名称是__________。
(2)上述框图中,①是__________反应,③是__________反应(填反应类型)。
(3)化合物E是重要的工业原料,写出由D生成E的化学方程式:______________________。
(4)C2的结构简式是_________________________________,F1的结构简式是__________________________________________,F1和F2互为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。回答下列问题:
(1)氮原子价层电子对的轨道表达式(电子排布图)为_____________。
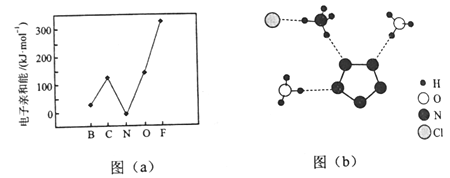
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是___________;氮元素的E1呈现异常的原因是__________。
(3)经X射线衍射测得化合物R的晶体结构,其局部结构如图(b)所示。
①从结构角度分析,R中两种阳离子的相同之处为_________,不同之处为__________。(填标号)
A.中心原子的杂化轨道类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子N5-中的σ键总数为________个。分子中的大π键可用符号![]() 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为![]() ),则N5-中的大π键应表示为____________。
),则N5-中的大π键应表示为____________。
③图(b)中虚线代表氢键,其表示式为(NH4+)N-H┄Cl、____________、____________。
(4)R的晶体密度为d g·cm-3,其立方晶胞参数为a nm,晶胞中含有y个[(N5)6(H3O)3(NH4)4Cl]单元,该单元的相对质量为M,则y的计算表达式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com