
��10�֣���ij�ֺ�������FeCl2���ʵ�FeCl3��Ʒ����Ҫ�ⶨ������Ԫ�ص�����������ʵ��������в�����У�
��ȷ����mg��Ʒ����2��3g��Χ�ڣ���
������Ʒ�м���10mL 6 moL��L��1�����ᣬ�ټ�������ˮ�����Ƴ�250mL��Һ��
����ȡ25mL����������õ���Һ������3mL��ˮ������ʹ�䷴Ӧ��ȫ��
�ܳ���Ѹ�ټ���10%��ˮ����������ֽ��裬ʹ������ȫ��
�ݹ��ˣ�������ϴ�Ӻ��������������ա���ȴ�����أ����ظ����������ء�
�Իش��������⣺
��1���ܽ���Ʒʱ��Ҫ�������ᣬԭ���� ��
��2��������ˮ��Ӧ�����ӷ���ʽΪ ��
��3�����������ˮ���ɳ��������ӷ���ʽΪ ��
��4����������ˮ�����������Լ��е� ���棨����ţ���
A��H2O2 B����ˮ C��NaClO
��5��������м�������Ƿ�ϴ���ķ����� ��
��6������������ΪW1g�����������պ�Ĺ���������ΪW2g����Ʒ����Ԫ�ص���������Ϊ ����ѽ��Լ�����
��1������Fe2+��Fe3+��ˮ�⣨1�֣� ��2��2Fe2+ + Cl2= 2Fe3+ + 2Cl����1�֣�
��3��Fe3+ + 3NH3��H2O = Fe(OH)3�� + 3NH4+��2�֣� ��4��AC��2�֣�
��5��ȡ���һ��ϴ��Һ���Թ��У�����AgNO3��Һ����Һ������ǣ�˵������ϴ�Ӹɾ�����2�֣�
��6��[7��W2��W1��/10m]��100%��2�֣�
��������
�����������1��FeCl2��FeCl3����ǿ�������Σ�����Һ��������ˮ�ⷴӦ��Ϊ������Fe2+��Fe3+��ˮ�⣬�ܽ���Ʒʱ��Ҫ���������2�������������ԣ���FeCl2�л�ԭ�ԣ����ᷢ��������ԭ��Ӧ�����Լ�����ˮ��Ӧ�����ӷ���ʽΪ2Fe2+ + Cl2= 2Fe3+ + 2Cl������3������Fe3+����Һ�м��������ˮ�ᷢ�����ֽⷴӦ������Fe(OH)3����,��Ӧ�����ӷ���ʽΪFe3+ + 3NH3��H2O = Fe(OH)3�� + 3NH4+����4����������ˮ������Fe2+����ΪFe3+������������H2O2��NaClOѡ����A��C����5���ڲ������Fe(OH)3�����ǴӺ���Cl-����Һ�й��˳����ģ�������ϴ�Ӹɾ�����ϴ����Һ����Cl-,���Լ�������Ƿ�ϴ���ķ�����ȡ���һ��ϴ��Һ���Թ��У�����AgNO3��Һ����Һ������ǣ�˵������ϴ�Ӹɾ�����6������������ΪW1g�����������պ�Ĺ���������ΪW2g����m(Fe2O3)=(W2��W1)g,��Ʒ����Ԫ�ص���������Ϊ{[(W2��W1)g��160g/mol]��2��56g/mol}��mg��100%=[7��W2��W1��/10m]��100%.
���㣺���鷴Ӧ�����Ŀ��ơ��ε�ˮ�⡢���ӷ���ʽ����д������ϴ�ӵķ��������ʺ����IJⶨ��֪ʶ��


 �����Ļ������������������ϵ�д�
�����Ļ������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ��У������ѧ�ڵ�һ���������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ˮ��Һ���ܴ��������һ��������
A��NH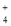 ��Na+��Cl����SO
��Na+��Cl����SO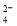 B��K����Mg2����OH����NO
B��K����Mg2����OH����NO
C��H����Ca 2����SiO ��NO3�� D��K����Al3����ClO����HCO3��
��NO3�� D��K����Al3����ClO����HCO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ������ѧ�ڵڶ����¿�������ѧ�Ծ��������棩 ���ͣ�ѡ����
2011��9 ��29�գ���������2F�����ػ���ɹ������칬һ�š�Ŀ�����������̫�գ������ʹ�õ�ȼ����ƫ�����£�CH3��NH��NH��CH3����������������N2O4�����ڻ�����չ����У�ȼ�Ϸ�����Ӧ��CH3��NH��NH��CH3��2N2O4��2CO2��3N2��4H2O�ṩ����������������ȷ����
A����ȼ����ɫ��������ȼ�չ����в�������κλ�����Ⱦ
B���÷�Ӧ��N2O4����������ƫ�������ǻ�ԭ��
C��CO2���������N2�ǻ�ԭ����
D��ÿ��0.6 mol N2���ɣ�ת�Ƶ�����ĿΪ2.4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ���и���10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ֽ�1mo1Cu2S��144��FeOͶ�뵽����ϡ������Һ�У���ַ�Ӧ�õ�Fe(NO3)3��Cu(NO3)2 ��CuSO4�Ļ����Һ��������NO���塣�����շ�Ӧ����NO���ʵ���Ϊ
A��4 mo1 B��5 mo1 C��6 mo1 D��7 mo1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ���и���10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��36.5����Ũ����(�ܶ�1.2 g��cm��3)��1 mol��L��1��ϡ���� 100 mL�����ƹ������õ���Щ���������Ⱥ�˳����ȷ���Ǣ�100 mL��Ͳ ��10 mL��Ͳ ��50 mL �ձ� ��������ƽ ��100 mL����ƿ��ͷ�ι� �߲�����
A���٢ۢݢޢ� B���ڢۢߢݢ� C���ۢݢߢޢ� D���ܢۢߢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ�����и�����ѧ������������ѧ�Ծ���A���������棩 ���ͣ�ѡ����
��ѧ�ļ���������ǿ�ѧ̽�����ȵ��ͼ�ֵ���ڡ������м��裨���룩�����µ�̽���϶�û���������
A��̽��SO2��Na2O2��Ӧ������Na2SO4����
B��̽��Na��ˮ�ķ�Ӧ��������NaOH��H2O2
C��̽��ŨH2SO4��ͭ��һ�������·�Ӧ�����ĺ�ɫ�����п�����CuS
D��̽������з�̪��Һ��NaOH��Һ��ͨ��Cl2����̪��ɫ��ȥ����������Һ������Ա仯���£�����HClO��Ư����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ�����и�����ѧ������������ѧ�Ծ���A���������棩 ���ͣ�ѡ����
����˵����ȷ����
A��HClO����Ԫ�ػ��ϼ۱�HClO4����Ԫ�ػ��ϼ۵ͣ����ԣ�HClO4��������ǿ
B����֪��Fe + Cu2+ = Fe2+ + Cu���� 2Fe3+ + Cu = 2Fe2+ + Cu2+����������ǿ��˳��Ϊ��Fe3+ > Cu2�� > Fe2+
C����֪��ԭ�ԣ�B�� > C��> D������Ӧ 2C�� + D2 = 2D�� +C2�ͷ�Ӧ 2C��+ B2=2B��+C2���ܷ���
D������ǿ�����Ժ�ǿ��ԭ�Ե����ʷ���һ����ܷ���������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ������ѧ�ڵ�һ��������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��������ʵ�������ȷ���� ( )
A��Ư����Һ�ڿ�����ʧЧ��ClO����CO2��H2O =HClO��HCO3-
B����Ũ������MnO2��Ӧ��ȡ���������� MnO2��2H����2Cl�� 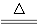 Mn2����Cl2����2H2O
Mn2����Cl2����2H2O
C����С�մ�����θ����ࣺHCO3-+H+=CO2��+H2O
D����ǿ����Һ�д���������Fe(OH)3��Ӧ����Na2FeO4��
3ClO����2Fe(OH)3 =2FeO42-��3Cl����H2O��4H��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ��̨�и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
(16��)ij��ѧС����ʵ����������CaSO4��NH3��CO2�Ʊ�(NH4)2SO4���乤���������¡�

�ش��������⣺
��1��������һϵ�в�����������Ũ����_______�����ˡ���������ʢװCaCO3��������___(������)��
��2��X����Ϊ_______(�ѧʽ����ͬ)��Y����Ϊ_____����ѭ�����õ����ʵ���_______________��
��3������װ�ò�������ʵ�����ư�������________________(�����)��
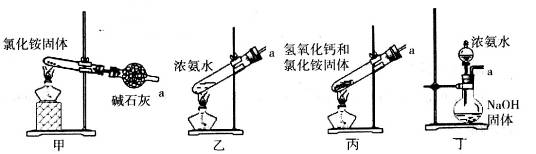
��4���û�ѧС����װ����ͼ��ʾװ����̽��NH3�Ļ�ԭ�ԡ��þƾ��Ƽ���C��Ӳ���Թ�һ��ʱ���D�в�������������ͨ��C����һ�᳷ȥC���ƾ��ơ�
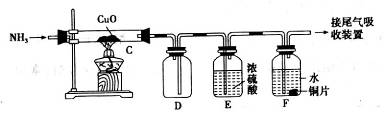
��ʵ�������F��ͭƬû���κα仯��D������������ֻ�۲쵽C�к�ɫ��ĩ��죬��C�з�����Ӧ�Ļ�ѧ����ʽΪ___________________________________________��
��ʵ�������C��ֻ�۲쵽��ɫ��ĩ��죬F��ͭƬ���ܽ⣬��
��D�й۲쵽��������__________________________________________________��
��F��ͭƬ���ܽ��ԭ����______________________________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com