
 2C(g)+2D(g) ��H��2minĩ�ﵽƽ�⣬����0.8mol D��
2C(g)+2D(g) ��H��2minĩ�ﵽƽ�⣬����0.8mol D�� =____________��
=____________��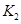 =l�����H________0���>����<������
=l�����H________0���>����<������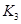 �� ��K3________
�� ��K3________ �����<����>����=������ԭ����_______________________��
�����<����>����=������ԭ����_______________________�� (A)=
(A)=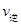 (C) D����������ܶȲ���
(C) D����������ܶȲ��� 2C(g)+2D(g)�ɿ�������ӦʱA ��B��C��D�����ʵ����Ĺ�ϵ��3��1��2��2����Ϊ����0.8mol��D����������A1.2mol������B0.4mol������C0.8mol����A��ƽ��Ũ��Ϊ����2-1.2��mol��2L="0.4mol�ML" . B��ת����Ϊ��0.4mol��2mol�� 100%="20%," 0-2min��D��ƽ����Ӧ����ΪV="��C�M" ��t="(0.8mol��2L)" �M2min=" 0.2" mol�M(L��min).(2)��ѧƽ�ⳣ���ǿ��淴Ӧ�ﵽ��ѧƽ��ʱ��������Ũ����ָ���Ļ������Ӧ��Ũ����ָ���Ļ�֮K={C2(C)C2(D) }�M{C3(A)C (B)}���ﵽ��ѧƽ��ʱ�����ʵ�Ũ�ȷֱ���C(A)=" 0.4mol�ML" ;C(B)="(2-0.4)mol��2L=0.8mol�ML" ;C(C)=" 0.8mol" ��2L="0.4" mol�ML ;C(D)=" 0.8mol" ��2L="0.4" mol�ML�����Ի�ѧƽ�ⳣ��Ϊ��K1={��0.4��2����0.4��2}�M{��0.4��3��0.8}=0.5.����Ϊ��350��ʱK2=l���ɼ������¶ȣ�K����˵�������¶Ȼ�ѧƽ��������Ӧ�����ƶ������ݻ�ѧƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ���������Ӧ�����ȷ�Ӧ���ʡ�H>0.��3������Ӧ�������ѹ����Ҳ��������ѹǿ�����ݻ�ѧƽ���ƶ�ԭ��������ѹǿ����ѧƽ�������������С�ķ����ƶ������÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ����������ѹǿ����ѧƽ�ⲻ�ƶ�����ʱA��B��ת�����ʶ����ᷢ���仯����ѧƽ�ⳣ��ֻ���¶��йء���������Ͷ�ϵĶ��ټ������ء�����K1=K3. (4)����Ӧ�ﵽ��ѧƽ��ʱ�����ʵ�Ũ�Ȳ��䣬��ͬһ���ʱ�ʾ������Ӧ���ʺ��淴Ӧ������ȣ������ʵĺ������䡣����������������䣬�÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ�������κ�ʱ��ѹǿ���䣬������ܶ�Ҳ���䣬�����Dz�����Ϊ�ж�ƽ��ı�־����ȷѡ��Ϊ��B��
2C(g)+2D(g)�ɿ�������ӦʱA ��B��C��D�����ʵ����Ĺ�ϵ��3��1��2��2����Ϊ����0.8mol��D����������A1.2mol������B0.4mol������C0.8mol����A��ƽ��Ũ��Ϊ����2-1.2��mol��2L="0.4mol�ML" . B��ת����Ϊ��0.4mol��2mol�� 100%="20%," 0-2min��D��ƽ����Ӧ����ΪV="��C�M" ��t="(0.8mol��2L)" �M2min=" 0.2" mol�M(L��min).(2)��ѧƽ�ⳣ���ǿ��淴Ӧ�ﵽ��ѧƽ��ʱ��������Ũ����ָ���Ļ������Ӧ��Ũ����ָ���Ļ�֮K={C2(C)C2(D) }�M{C3(A)C (B)}���ﵽ��ѧƽ��ʱ�����ʵ�Ũ�ȷֱ���C(A)=" 0.4mol�ML" ;C(B)="(2-0.4)mol��2L=0.8mol�ML" ;C(C)=" 0.8mol" ��2L="0.4" mol�ML ;C(D)=" 0.8mol" ��2L="0.4" mol�ML�����Ի�ѧƽ�ⳣ��Ϊ��K1={��0.4��2����0.4��2}�M{��0.4��3��0.8}=0.5.����Ϊ��350��ʱK2=l���ɼ������¶ȣ�K����˵�������¶Ȼ�ѧƽ��������Ӧ�����ƶ������ݻ�ѧƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ���������Ӧ�����ȷ�Ӧ���ʡ�H>0.��3������Ӧ�������ѹ����Ҳ��������ѹǿ�����ݻ�ѧƽ���ƶ�ԭ��������ѹǿ����ѧƽ�������������С�ķ����ƶ������÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ����������ѹǿ����ѧƽ�ⲻ�ƶ�����ʱA��B��ת�����ʶ����ᷢ���仯����ѧƽ�ⳣ��ֻ���¶��йء���������Ͷ�ϵĶ��ټ������ء�����K1=K3. (4)����Ӧ�ﵽ��ѧƽ��ʱ�����ʵ�Ũ�Ȳ��䣬��ͬһ���ʱ�ʾ������Ӧ���ʺ��淴Ӧ������ȣ������ʵĺ������䡣����������������䣬�÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ�������κ�ʱ��ѹǿ���䣬������ܶ�Ҳ���䣬�����Dz�����Ϊ�ж�ƽ��ı�־����ȷѡ��Ϊ��B��

 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д� �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
2SO3(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���| t/s | 0 | t1 | t2 | t3 | t4 |
| n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3�տ�ʼʱ��N2��Ũ��Ϊ3 mol/L��H2��Ũ��Ϊ5 mol/L��3 min����NH3Ũ��Ϊ0.6 mol/L�����ʱ���ڣ����з�Ӧ���ʱ�ʾ��ȷ����
2NH3�տ�ʼʱ��N2��Ũ��Ϊ3 mol/L��H2��Ũ��Ϊ5 mol/L��3 min����NH3Ũ��Ϊ0.6 mol/L�����ʱ���ڣ����з�Ӧ���ʱ�ʾ��ȷ���� | A��v(NH3)="0.2" mol/��L��s�� | B��v(N2)="1.0" mol/��L��min�� |
| C��v(H2)="1.67" mol/��L��min�� | D��v(H2)="0.3" mol/��L��min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 2NH3(g) ��2 minʱ�ﵽƽ��״̬����ʱc(N2)��5.00 mol/L��c(H2)��10.00mol/L��c(NH3)��5.00 mol/L������д��������̣�
2NH3(g) ��2 minʱ�ﵽƽ��״̬����ʱc(N2)��5.00 mol/L��c(H2)��10.00mol/L��c(NH3)��5.00 mol/L������д��������̣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 PCl3+Cl2��һ��ʱ�����PCl5��Ũ��Ϊ0.3mol��L�������ʱ���ڵ�ƽ����Ӧ����v(PCl5)="0.4" mol��(L��min)�������ʱ��Ϊ
PCl3+Cl2��һ��ʱ�����PCl5��Ũ��Ϊ0.3mol��L�������ʱ���ڵ�ƽ����Ӧ����v(PCl5)="0.4" mol��(L��min)�������ʱ��Ϊ| A��80s | B��45s | C��30s | D��15s |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ?2AB3��Ӧ��˵�����·�Ӧ���ʱ�ʾ��Ӧ�����ǣ� ��
?2AB3��Ӧ��˵�����·�Ӧ���ʱ�ʾ��Ӧ�����ǣ� ��| A��v(AB3)��0.5 mol/(L��min) | B��v(B2)��0.6 mol/(L��min) |
| C��v(A2)��0.4 mol/(L��min) | D�����ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C��g��+D��g������ij��ʱ���ڣ���A��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ2 mol/��L��s��������C��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ
2C��g��+D��g������ij��ʱ���ڣ���A��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ2 mol/��L��s��������C��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ| A��1 mol/��L��s�� | B��3 mol/��L��s�� |
| C��4 tool/��L��s�� | D��2 mol/��L��s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.1 mol��L-1��min-1 | B��0.3 mol��L-1��min-1 |
| C��0.2 mol��L-1��min-1 | D��0.6 mol��L-1��min-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com