
ЎҫМвДҝЎҝДі»ҜС§РЛИӨРЎЧйОӘМҪҫҝФӘЛШРФЦКөДөЭұд№жВЙЈ¬ЙијЖБЛИзПВПөБРКөСйЈ®
ЈЁ1Ј©ўсЈ®Ҫ«ДЖЎўјШЎўГҫЎўВБёч1mol·ЦұрН¶ИлөҪЧгБҝөД0.1molL©Ғ1өДСОЛбЦРЈ¬КФФӨІвКөСйҪб№ыЈәУлСОЛб·ҙУҰЧоҝмЈ®
ЈЁ2Ј©ўтЈ®АыУГПВНјЧ°ЦГҝЙТФСйЦӨ·ЗҪрКфРФөДұд»Ҝ№жВЙЈ® 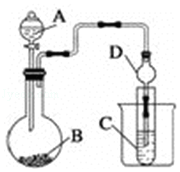
ТЗЖчAөДГыіЖОӘ Ј¬ ёЙФп№ЬDөДЧчУГКЗ Ј®
ЈЁ3Ј©ИфТӘЦӨГч·ЗҪрКфРФЈәSЈҫCЈҫSiЈ¬ФтAЦРјУЎўBЦРјУNaHCO3ИЬТәЎўCЦРјУ Ј¬ №ЫІмөҪCЦРИЬТәөДПЦПуОӘ Ј®
Ўҫҙр°ёЎҝ
ЈЁ1Ј©K
ЈЁ2Ј©·ЦТәВ©¶·Ј»·АЦ№ө№Оь
ЈЁ3Ј©ПЎБтЛбЈ»Na2SiO3ИЬТәЈ»ИЬТәұд»лЧЗ
ЎҫҪвОцЎҝҪвЈәIЎўЈЁ1Ј©Н¬Т»ЦЬЖЪФӘЛШЈ¬ҪрКфРФЛжЧЕФӯЧУРтКэФцҙу¶шјхИхЈ¬ФӘЛШөДҪрКфРФФҪЗҝЈ¬Н¬Т»ЦчЧеЈ¬ФӯЧУРтКэФҪҙуЈ¬ҪрКфРФФҪЗҝЈ¬ЖдөҘЦКУлЛб»тЛ®·ҙУҰФҪҫзБТЈ¬ЛщТФҪрКфРФKЈҫNaЈҫMgЈҫAlЈ¬ФтKУлСОЛб·ҙУҰЧоҫзБТЈ¬ЛщТФҙр°ёКЗЈәKЈ»ўтЈ®ЈЁ2Ј©ТЗЖчAОӘ·ЦТәВ©¶·Ј¬ЗтРОёЙФп№ЬDДЬ№»·АЦ№ө№ОьЈ¬ҝЙТФұЬГвCЦРТәМеҪшИлЧ¶РОЖҝЦРЈ¬ЛщТФҙр°ёКЗЈә·ЦТәВ©¶·Ј»·АЦ№ө№ОьЈ»ЈЁ3Ј©ИфТӘЦӨГч·ЗҪрКфРФЈәCЈҫSiЈ¬ҝЙТФНЁ№э¶юСх»ҜМјәН№иЛбДЖ·ҙУҰЙъіЙДСИЬРФөД№иЛбАҙЦӨГчЈ¬УЙУЪBЦРјУNaHCO3 Ј¬ №КAЦРҝЙТФјУБтЛбЈ¬НЁ№эБтЛбәНМјЛбЗвДЖөД·ҙУҰАҙЦЖИЎCO2 Ј¬ И»әуөДCO2НЁИлCЦРөДNa2SiO3ЦРЈ¬ҝЙТФ·ўЙъ·ҙУҰЈәNa2SiO3+2CO2+2H2O=H2SiO3Ўэ+2NaHCO3 Ј¬ АлЧУ·ҙУҰОӘЈәSiO32©Ғ+2CO2+2H2O=H2SiO3Ўэ+2HCO3©Ғ Ј¬ ІъЙъ°ЧЙ«ҪәЧҙіБөнЈ¬ҙУ¶шҝЙТФЦӨГчЛбРФЈәH2CO3ЈҫH2SiO3 Ј¬ №К·ЗҪрКфРФЈәCЈҫSiЈ®ЛщТФҙр°ёКЗЈәПЎБтЛбЈ»Na2SiO3ИЬТәЈ»ИЬТәұд»лЧЗЈ®



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРОўБЈФЪИЬТәЦРДЬҙуБҝ№ІҙжөДКЗ
A.NH4+ЎўFe2Ј«ЎўSO42-ЎўNO3-B.Mg2Ј«ЎўKЈ«ЎўClЈӯЎўAlO2-
C.Al3Ј«ЎўNaЈ«ЎўSO42-ЎўHSЈӯD.Ca2Ј«ЎўHЈ«ЎўNO3- ЎўSO32-
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРіЈјыОпЖ·ЦРЦчТӘУЙМмИ»УР»ъІДБПЦЖіЙөДКЗЈЁ Ј©
A. І»РвёЦ№ш B. ІПЛҝЛҝҪн C. ЛЬБПЕи D. ІЈБ§ұӯ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРЛө·Ё»тұнКҫ·Ҫ·ЁЦРЈ¬ХэИ·өДКЗЈЁ Ј© 
A.өИЦКБҝөДБтХфЖшәНБт№ММе·ЦұрНкИ«ИјЙХЈ¬З°ХЯ·ЕіцөДИИБҝЙЩ
B.ИзНјҝЙұнКҫCәНH2OЈЁgЈ©·ҙУҰ№эіМЦРөДДЬБҝұд»Ҝ
C.ОьИИ·ҙУҰТ»¶ЁТӘјУИИЈ¬ІЕДЬҪшРР
D.ТСЦӘЦРәНИИОӘ57.3 kJmol©Ғ1 Ј¬ ФтЕЁБтЛбУлNaOHИЬТә·ҙУҰЙъіЙ 1mol H2OКұЈ¬№І·Еіц57.3 kJөДДЬБҝ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБР№ШУЪ»ҜС§КөСй»щұҫІЩЧчөДРрКцЦРЈ¬ХэИ·өДКЗ
A. јУИИХф·ўКұЈ¬Хф·ўГуұШРлөжКҜГЮНш
B. ЦЖFe(OH)3ҪәМеКұЈ¬Ҫ«ұҘәНFeCl3ИЬТәјУИИЦу·Р
C. ·ЦТәКұЈ¬·Еіц·ЦТәВ©¶·ПВІгТәМеәуЈ¬ФЩјМРш·ЕіцЙПІгТәМе
D. ХфБуКұЈ¬ФЪЙХЖҝЦРјУИл·РКҜ»тЛйҙЙЖ¬Ј¬ТФ·АЦ№ТәМеұ©·Р
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРОпЦКөД№ӨТөЦЖұёФӯАнІ»Йжј°Сх»Ҝ»№Фӯ·ҙУҰөДКЗЈЁ Ј©
A. УГҪ№МҝәНКҜУўЦЖұёҙЦ№и
B. әЈЛ®Мбде
C. УГУНЦ¬әНNaOHИЬТәЦЖұё·КФн
D. АыУГВБИИ·ҙУҰЦЖұёҪрКфГМ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіС§ЙъөДКөСйұЁёжЛщБРіцөДПВБРКэҫЭЦРәПАнөДКЗ
A. УГ10mLБҝНІБҝИЎ7.13 mLПЎСОЛб
B. УГНРЕММмЖҪіЖБҝ25.20g NaCl
C. УГ№г·әpHКФЦҪІвөГДіИЬТәөДpHОӘ2.3
D. УГ25mLөО¶Ё№ЬЧцЦРәНөО¶ЁКұЈ¬УГИҘДіЕЁ¶ИөДјоИЬТә21.70mL
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝАаұИНЖАнКЗ»ҜС§ЦРіЈУГөДЛјО¬·Ҫ·ЁЈ¬ПВБРНЖАнХэИ·өДКЗЈЁ Ј©
A. SiH4өД·РөгёЯУЪCH4Ј¬НЖІвHClөД·РөгёЯУЪHF
B. NaФЪO2ЦРИјЙХЙъіЙNa2O2Ј¬НЖІвLiФЪO2ЦРИјЙХЙъіЙLi2O2
C. FeіЈОВПВФЪЕЁПхЛбЦР¶Ы»ҜЈ¬НЖІвCuіЈОВПВФЪЕЁПхЛбЦР¶Ы»Ҝ
D. SO2УлH2O2·ҙУҰЙъіЙH2SO4Ј¬НЖІвSO2УлNa2O2·ҙУҰЙъіЙNa2SO4
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРРрКцҙнОуөДКЗЈЁ Ј©
A.10mLЦКБҝ·ЦКэОӘ98%өДH2SO4 Ј¬ УГ10mLЛ®ПЎКНәуЈ¬H2SO4өДЦКБҝ·ЦКэҙуУЪ49%
B.ЕдЦЖ0.1mol/LөДNa2CO3ИЬТә480mLЈ¬РиУГ500mLИЭБҝЖҝ
C.ФЪұкҝцПВЈ¬Ҫ«22.4L°ұЖшИЬУЪ1LЛ®ЦРЈ¬өГөҪ1mol/LөД°ұЛ®
D.Н¬ОВН¬С№ПВЈ¬20mLCH4әН60mLO2Лщә¬өДФӯЧУКэЦ®ұИОӘ5Јә6
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com