
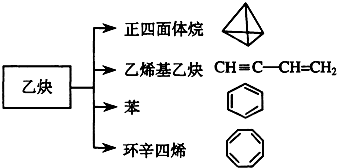
| A、正四面体烷的二氯取代产物有2种 |
| B、正四面体烷与乙烯基乙炔互为同分异构体 |
| C、苯与环辛四烯互为同系物 |
| D、等质量的苯与环辛四烯完全燃烧消耗氧气量不相同 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
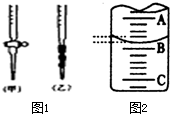
| A、滴定管用水洗后,未用标准溶液润洗就装入标准溶液 |
| B、锥形瓶盛待测液前,用待测液润洗 |
| C、读数时,滴定前仰视,滴定后俯视 |
| D、滴定结束后,发现碱式滴定管尖嘴处悬挂一滴碱液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.52 | 25.42 |
| 第二次 | 20.00 | 4.07 | 29.17 |
查看答案和解析>>
科目:高中化学 来源: 题型:
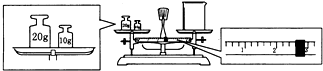 实验室欲用NaOH固体配制1.0mol?L-1的NaOH溶液240mL.
实验室欲用NaOH固体配制1.0mol?L-1的NaOH溶液240mL.查看答案和解析>>
科目:高中化学 来源: 题型:
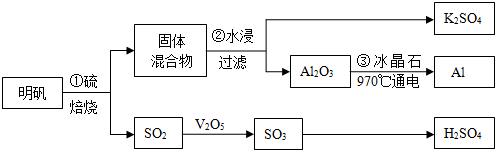
查看答案和解析>>
科目:高中化学 来源: 题型:
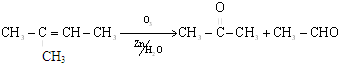 从石油分馏产品C8H18制取二氢茉莉酮酸甲酯(香料)的流程如图:(备注:E是D的一元取代物)
从石油分馏产品C8H18制取二氢茉莉酮酸甲酯(香料)的流程如图:(备注:E是D的一元取代物)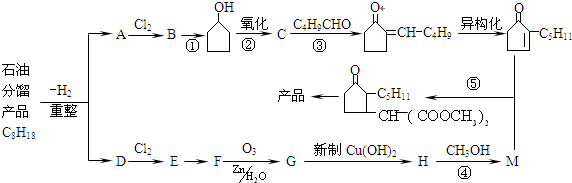
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2晶体中阴阳离子个数比2:1 |
| B、0.2mol?L-1的CH3COOH溶液与0.1mol?L-1CH3COOH溶液中c(H+)之比 |
| C、pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH4+)与c(SO42-)之比 |
| D、pH=11的Ba(OH)2溶液与pH=12的KOH溶液中溶质的物质的量浓度之比 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com