
| A、CH3-(CH2)4-CH3 |
| B、CH3-(CH2)3-CH3 |
| C、CH3-CH2-CH(CH3)2 |
| D、(CH3)2C(CH3)2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | T | X | Y | Z |
| 性质 结构 信息 | 人体内含量最多的元素,且其单质是常见的助燃剂. | 单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼. | 常温下单质能与水剧烈反应生成氢气. | 第三周期元素的简单离子中半径最小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
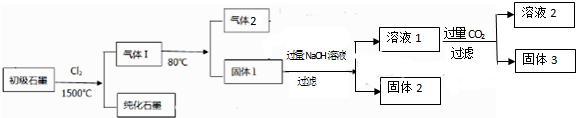
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH4+Cl2
| |||
B、nCH2═CH2
 | |||
C、 +HO-NO2 +HO-NO2
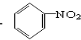 +H2O +H2O | |||
D、2CH3CH2OH+O2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ag2SO4>AgCl>Ag2CO3>AgI |
| B、Ag2SO4>Ag2CO3>AgCl>AgI |
| C、Ag2SO4 >AgCl>AgI>Ag2CO3 |
| D、Ag2SO4>Ag2CO3>AgI>AgCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出 |
| B、实验室可用NaOH溶液处理NO2和HCl废气 |
| C、酸碱滴定时,若加入待测液前用待测液润洗锥形瓶,对测定结果无影响 |
| D、依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com