
【题目】某酸碱指示剂是一种有机弱酸,其在水溶液中呈现的颜色与其电离平衡相关:HA(红色)![]() H++A-(黄色),若要使该指示剂呈黄色,则应加入
H++A-(黄色),若要使该指示剂呈黄色,则应加入
A. H2SO4 B. HCl C. NaOH D. NaHSO4
科目:高中化学 来源: 题型:
【题目】下列关于铜电极的叙述中正确的是
A.用电解法精炼粗铜时纯铜作阴极
B.在铁上电镀铜时用铜作阴极
C.铜锌原电池中铜是负极
D.电解稀硫酸时用铜作阳极,阳极产生氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O与D2O的pKw(p/Cw=-lgKw)与温度的关系如图所示,下列有关说法正确的是
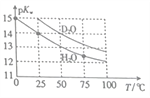
A. 常温下,向D2O中加入DCl,pKw变大
B. 25℃时,纯D2O的pH等于7
C. 25℃时,pH=7的液体一定是纯H2O
D. D2O的电离过程为吸热过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中D是一种饱和一元醇,其蒸气的密度是相同状况下氢气密度的23倍。请回答:
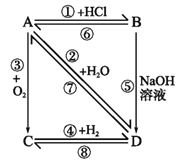
(1)写出结构简式:A_________,B_________, C________,D_________。
(2)指出反应类型:⑤________,⑧_________。
(3)指明反应条件:⑦_________________。
(4)写出化学方程式: ⑧____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是一种食品添加剂。实验室用如图所示装置制备Na2S2O5,实验步骤如下:

Ⅰ.向Na2CO3溶液中通入SO2至溶液pH为4.1,生成NaHSO3溶液;
Ⅱ.加入碳酸钠粉末至溶液PH为7~8;
Ⅲ.再通入SO2至溶液PH为4.1;
Ⅳ.从过饱和溶液中析出Na2S2O5晶体。
(1)制备焦亚硫酸钠总反应的化学方程式为___________________ 。
(2)Na2S2O5能与水发生化合反应,反应后所得的溶液显酸性。用电离方程式表示溶液显酸性的原因:____________________。
(3)利用碘量法可测定Na2S2O5产品中硫的含量。实验中必须使用的试剂有c1mol·L-1的标准碘溶液、c2 mol·L-1的标准Na2S2O3溶液、NaOH溶液、淀粉溶液。已知:Na2S2O5+2I2+3H2O=Na2SO4+H2SO4+4HI,2Na2S2O3+I2= Na2S2O6+2NaI。请补全实验方案:将一定量的Na2S2O5产品放入碘量瓶(带磨口塞的锥形瓶)中,加入—定体积的过量c1 mol L-1的标准碘溶液,充分反应后滴入NaOH溶液调节溶液pH至中性,____________________________。重复上述步骤2次,记录数据。
(4)含铬酸性废水中常含有+ 6价铬。利用Na2S2O5和FeSO4·7H2O分两个阶段先后处理含Cr2O72-的废水, Cr2O72-被还原为Cr3+,实验结果如图。

①0~40 min内用Cr2O72-表示的平均反应速率为____________mol L-1 min-1。
②60~80 min内Cr2O72-与Fe2+发生反应的离子方程式为_________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A(g)+4B(g) = 2C(g)+2D(g),下列数据表示反应进行得最快的是( )
A. v(A)=1.4mol/(L·s) B. v(B)=3.6mol/(L·s)
C. v(C)=2mol/(L·s) D. v(D)=3.0mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素的原子,前者一定大于后者的是( )
A. 中子数、质子数 B. 质量数、核电荷数
C. 最高正化合价数、负化合价数 D. 核外电子数、其阳离子核外电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A为含三种元素的钠盐,其水溶液显碱性.C为大理石的主要成分,请填空: 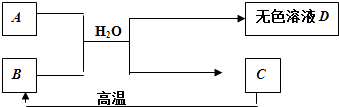
(1)C的化学式 .
(2)D中一定含有的溶质是 . 理由是(用化学方程式表示) .
(3)B用作食品干燥剂的原理: . (用化学方程式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com