
����Ŀ��ij��ѧ�о���ѧϰС�����������ͼ��ʾ��ʵ��װ�ã�Ŀ����������ˮ��Ӧ��ʵ������֤���Ƶ��������ʣ����ƺ�ˮ��Ӧ�IJ����ش��������⣺

��1��ʵ�鿪ʼʱ����ʹ����ˮ�Ӵ���Ӧ��Ӧ��β�����_______________ ��
��2����Ӧ��ʼ���Թ����ܹ۲쵽��ʵ�������ǣ�________����д������
A������ˮ���з�Ӧ�۳�С���Ĵ��ζ�
B��������Һ����洦��Ӧ�۳�С��������������
C������ˮ���з�Ӧ�۳�С���Ĵ��ζ�
D���Ʋ��ϵؼ�С����ʧ
E����ͣ����ú�Ͳ��в���Ӧ
F.ú���������ݲ���
��3��ͨ�����������ܹ���֤�Ƶ���Щ�������ʣ�________________
��4��100 mL ����ƿ��ʢ��100mL0.101mol/L��BaCl2��Һ����������ϡ�ͳ�Ũ��Ϊ0.100mol/L��BaCl2��Һ������Ա���Ϊ100mL��,��ѡ�õ������У�10mL��Ͳ��1mL��Һ������ȷ��ȡ0.10��1.00mL��Һ������ͷ�ιܡ���IJ���������__________��
���𰸡�
��1������ͷ���¶˵�������ˮ����
��2��B��D��F��
��3���ܶ�С���۵����
��4����1mL��Һ�ܴ�����ƿ����ȡ0.99mLBaCl2��Һ��Ȼ�����ý�ͷ�ι�С�ļ�����ˮ���̶��ߣ��Ǻ�ƿ����������תҡ�ȣ����õ�0.100mol/LLBaCl2��Һ ��
��������
�����������1��ʵ�鿪ʼʱ����ʹ����ˮ�Ӵ���Ӧ��ֻ��Ҫ����ͷ���¶˵�������ˮ�м��ɣ��ʴ�Ϊ������ͷ���¶˵�������ˮ�У�
��2����Ӧ��ʼ�� ������Һ����洦��Ӧ�۳�С�����������������Ʋ��ϵؼ�С����ʧ��ú���������ݲ�������ѡB��D��F��
��3��ͨ����������˵���Ƶ��ܶ�С���۵�ͣ��ʴ�Ϊ���ܶ�С���۵�ͣ�
��4����������100mL0.100molL-1��BaCl2��Һ�������0.1010molL-1��BaCl2��Һ�����ΪVmL��������Һϡ�Ͷ���CŨVŨ=CϡVϡ��֪��0.1010molL-1��VmL=100mL��0.100molL-1�����V=99.0mL������1mL��Һ���Ƴ�0.99mL��0.1010molL-1��BaCl2��Һ��Ȼ���ý�ͷ�ι���ʣ�µ�99.01mL 0.1010molL-1��BaCl2��Һ�м�ˮ���̶��ߣ�������תҡ�ȣ��������Ƶ�0.100molL-1��BaCl2��Һ��,�ʴ�Ϊ����1mL��Һ���Ƴ�0.99mL��0.1010molL-1��BaCl2��Һ��Ȼ���ý�ͷ�ι���ʣ�µ�99.01mL 0.1010molL-1��BaCl2��Һ�м�ˮ���̶��ߣ�������תҡ�ȣ��������Ƶ�0.100molL-1��BaCl2��Һ��


 ͬ��������ϰϵ�д�
ͬ��������ϰϵ�д� �ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
�ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�����Һ����������������еĹ�ͬ�����ǣ� ��
A.��ɢ������ֱ������1��100nm֮��
B.���ܲ��������ЧӦ
C.��©������ʱ��ֽ��û����������
D.���ʺ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������������Ȼ��г�ദ����
A�������г�����ȼ���������°�
B����̫���ܡ����ܡ�ˮ�ܵ���Դ�����ʯȼ��
C�������ϡ����л�������������뽭����
D��ʵʩ����ȼ���������������Լ������������ŷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������CO2ͨ��KOH��Ca��OH��2�Ļ����Һ�У����ɳ�����������m����ͨ��CO2�����V���Ĺ�ϵ��ͼ��ʾ��
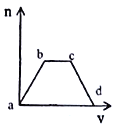
��1��ab�η��������ӷ�Ӧ����ʽΪ_____________��
��2��bc�����η����������ӷ�Ӧ��������_________�� �����___________��
��3��cd�η��������ӷ�Ӧ����ʽ��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ�������
A. 1s����ĵ�������״ΪԲ�ε���
B. 2s�ĵ����ư뾶��1s�����ư뾶��˵��2s�ܼ��ĵ��ӱ�1s�Ķ�
C. ������1s������˶������Χ��̫����ת
D. 4f�ܼ�����������14������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.���й��ۼ��Ļ�����һ���ǹ��ۻ�����
B.ֻ�������Ӽ��Ļ�����������ӻ�����
C.����ֻ�зǽ���ԭ�Ӽ�����γɹ��ۼ�
D.�ɹ��ۼ��γɵķ���һ���ǹ��ۻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������H2��һ���¶��¿ɷ�Ӧ����һ�ֽ��⻯��(NaH)�İ�ɫ������û�����������״̬�¿ɵ��磬ȡ����NaH����ˮ�У����ҷ�Ӧ�ų�һ����ɫ����ζ�����壬���γ�һ�ּ�����Һ��
��1��Na��H2��Ӧ�Ļ�ѧ����ʽΪ___________��H2��________����
��2��NaH��ˮ��Ӧ�Ļ�ѧ����ʽΪ____________��NaH��_________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������ȷ���ǣ� ��
A. ���ó���©���������ͺ�ˮ�Ļ��Һ
B. �ƾ���ʹ�ò������������ƾ�������ȼ��ʱ��������ʪ������
C. ��ʢ��Һ����Թܼ���ʱ��Ҫ��ͣ���ƶ��Թ�
D. ϴ������ƿ������ƿ���ú�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���Ҳⶨ̼���ƺ�̼�����ƻ������̼���Ƶ���������W(Na2CO3)����ȡ�˻����5.0g������ˮ�У����250mL��Һ��
������һ���������������û�ѧ��Ӧ��HCO3����CO32����ȫת��Ϊ��������������������������ɴ˼��������Ц�(Na2CO3)��
��1����ȡ100mL���ƺõ���Һ���ձ��У��μ�����������������Һ��HCO3����CO32����ȫת��Ϊ������Ӧѡ�õ��Լ��� (����)��
A��CaCl2��Һ B��MgSO4��Һ C��NaCl��Һ D��Ba(OH)2��Һ
��2�������ó�����ָ����������������Ϊmg���ɴ˿��Լ����(Na2CO3)������˲��У�����δ�����־ͳ��������æ�(Na2CO3) (�ƫ����ƫС������Ӱ�족)��
����������������������ȡ10.00mL���ƺõ���Һ������ϡ������Һ��Ӧ���ⶨ����������ͨ��״��(Լ20����1.01��105Pa)��������ɴ˼��������Ц�(Na2CO3)��
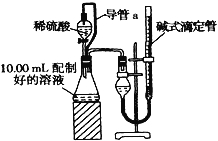
��1��װ���е���a�Ķ��������� ��
��2������ȥ����a��ʹ���������� (��ƫ����ƫС������Ӱ�족)��
�������������ζ�������ȡ25.00mL���ƺõ���Һ������ƿ�У��μ�2�η�̪�Լ���ҡ�ȣ���0.2000molL��1������ζ����յ�(��֪�յ�ʱ��ӦH++CO32���THCO3��ǡ����ȫ)���ظ��˲���2�Σ�������������ƽ��ֵΪ20.00mL��
��1����ȡ25.00mL���ƺõ���Һ��Ӧѡ�� ��������ɣ�
��2���жϵζ��յ�������� ��
��3���˷���æ�(Na2CO3)= %��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com