
| A. | 都能作干燥剂 | B. | 都具有一定的氧化性 | ||
| C. | 加热时都能与铜发生反应 | D. | 在常温下都能用铁制容器贮存 |
分析 A、浓硫酸具有吸水性,稀硫酸不具有吸水性;
B、浓硫酸具有强氧化性,稀硫酸具有弱氧化性;
C、加热时浓硫酸与铜发生反应,稀硫酸不与铜反应;
D、常温下浓硫酸与铁发生钝化,稀硫酸与铁反应生成硫酸亚铁和氢气;
解答 解:A、浓硫酸具有吸水性,稀硫酸不具有吸水性,所以浓硫酸能作干燥剂,稀硫酸不能,故A错误;
B、浓硫酸具有强氧化性,稀硫酸具有弱氧化性,所以都具有一定的氧化性,故B正确;
C、加热时浓硫酸与铜发生反应生成硫酸铜、二氧化硫和水,稀硫酸不与铜反应,故C错误;
D、常温下浓硫酸与铁发生钝化能用铁制容器贮存,稀硫酸与铁反应生成硫酸亚铁和氢气不能用铁制容器贮存,故D错误;
故选:ACD.
点评 本题考查浓硫酸、稀硫酸的性质,难度不大,注意基础知识的积累.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
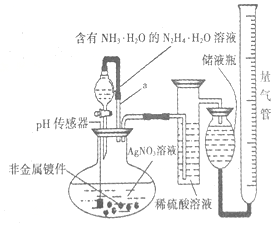 化学镀银法是非金属表面镀银的常用方法,如图是研究化学镀银中银元素利用率的实验装置(夹持仪器略):
化学镀银法是非金属表面镀银的常用方法,如图是研究化学镀银中银元素利用率的实验装置(夹持仪器略): .已知稀硝酸的氧化性强于Ag+,NH3•H2O中加适量氨水的一个重要目的是控制溶液的pH在8-9之间,简述溶液不能呈酸性的理由如果溶液呈酸性,被还原的是HNO3,而得不到银单质,从而导致实验失败.
.已知稀硝酸的氧化性强于Ag+,NH3•H2O中加适量氨水的一个重要目的是控制溶液的pH在8-9之间,简述溶液不能呈酸性的理由如果溶液呈酸性,被还原的是HNO3,而得不到银单质,从而导致实验失败.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应完全停止 | B. | 各物质的浓度保持不变 | ||
| C. | 反应物消耗完全 | D. | 正反应速率大于逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某化学课外兴趣小组为探究铜与浓硫酸反应气体产物的性质,拟用如图所示的装置的组合进行实验.
某化学课外兴趣小组为探究铜与浓硫酸反应气体产物的性质,拟用如图所示的装置的组合进行实验.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| A | B | ||
| D | E | G | J |
| L | M | Q |
 .写出一个能表示元素G、J非金属性强弱关系的化学方程式H2S+Cl2=2HCl+S↓或Na2S+Cl2=2NaCl+S↓.
.写出一个能表示元素G、J非金属性强弱关系的化学方程式H2S+Cl2=2HCl+S↓或Na2S+Cl2=2NaCl+S↓.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
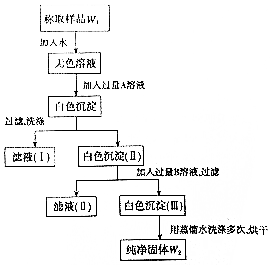 实验室有一瓶已部分被氧化的亚硫酸钠固体,为测定亚硫酸钠的质量分数,某同学设计如图所示实验.请根据实验步骤填写下列空白.
实验室有一瓶已部分被氧化的亚硫酸钠固体,为测定亚硫酸钠的质量分数,某同学设计如图所示实验.请根据实验步骤填写下列空白.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com