
| A. | Cu与浓硝酸反应制NO2:Cu+4HNO3(浓)═Cu2++2NO3-+2NO2↑+2H2O | |
| B. | 向Fe(NO3)2溶液中加入盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O | |
| C. | 碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| D. | 向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- |
分析 A.铜与浓硝酸反应生成硝酸铜、二氧化氮和水,浓硝酸应该拆开;
B.酸性条件下硝酸根离子能够将亚铁离子氧化成铁离子,同时硝酸根离子被氧化成NO气体;
C.石灰水少量,离子方程式按照氢氧化钙的化学式组成书写,反应产物中含有碳酸根离子;
D.二氧化碳过量,飞已售出碳酸氢根离子.
解答 解:A.Cu与浓硝酸反应制NO2,浓硝酸需要拆开,正确的离子方程式为:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O,故A错误;
B.向Fe(NO3)2溶液中加入盐酸,发生氧化还原反应,反应的离子方程式为:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,故B正确;
C.碳酸氢钠溶液与少量石灰水反应,离子方程式按照氢氧化钙的化学式组成书写,正确的离子方程式为:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O,故C错误;
D.向Na2SiO3溶液中通入过量CO2,反应生成硅酸沉淀和碳酸氢钠,正确的离子方程式为:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3-,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式等;试题侧重基础知识的考查,有利于提高学生的分析能力及灵活应用能力.


 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:选择题
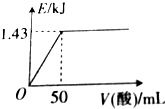 向50mL0.5mol•L-1NaOH溶液中加入某种浓度的稀硫酸,测得加入稀硫酸的体积与反应放出的热量关系如图所示(不考虑热量损失),该稀硫酸中硫酸的物质的量浓度为( )
向50mL0.5mol•L-1NaOH溶液中加入某种浓度的稀硫酸,测得加入稀硫酸的体积与反应放出的热量关系如图所示(不考虑热量损失),该稀硫酸中硫酸的物质的量浓度为( )| A. | 0.5mol•L-1 | B. | 0.4mol•L-1 | C. | 0.25mol•L-1 | D. | 0.1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 (其中一种)(写结构简式,一种即可).
(其中一种)(写结构简式,一种即可). +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$ +NaCl
+NaCl +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl;反应④是取代反应 (填反应类型).
+HCl;反应④是取代反应 (填反应类型).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ②③④ | C. | ②④⑤ | D. | 全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸铵溶液和盐酸反应:CH3COONH4+H+═CH3COOH+NH4+ | |
| B. | 碳酸氢铵溶液和过量氢氧化钠溶液:NH4++OH-═NH3•H2O | |
| C. | 偏铝酸钠溶液和过量盐酸:AlO2-+4H+═Al3++2H2O | |
| D. | 钠跟水反应:Na+2H2O═Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
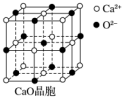 可以由下列反应合成三聚氰胺:CaO+3C$\frac{\underline{\;高温\;}}{\;}$CaC2+CO↑,CaC2+N2$\frac{\underline{\;高温\;}}{\;}$CaCN2+C,CaCN2+2H2O═NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺.
可以由下列反应合成三聚氰胺:CaO+3C$\frac{\underline{\;高温\;}}{\;}$CaC2+CO↑,CaC2+N2$\frac{\underline{\;高温\;}}{\;}$CaCN2+C,CaCN2+2H2O═NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺.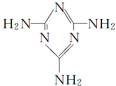 )俗称“蛋白精”,三聚氰酸(
)俗称“蛋白精”,三聚氰酸( 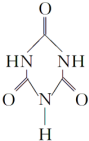 ).
).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物 | |
| B. | Na2O、NaOH、Na2CO3、NaCl、Na2SO4、Na2O2都属于钠的含氧化合物 | |
| C. | 漂白粉、福尔马林、冰水、王水、氯水均为混合物 | |
| D. | HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 步骤①中发生的主要反应为Cl2+2Br-═Br2+2Cl- | |
| B. | 步骤②③的目的是富集溴元素 | |
| C. | 物质X 为HBrO | |
| D. | 空气吹出法用到了溴易挥发的性质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com