
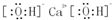 £®
£®·ÖĪö £Ø1£©ČōX”¢W¾łĪŖµ„ÖŹ£¬Y”¢Z¾łĪŖŃõ»ÆĪļ£¬ÕāĖµĆ÷ĪŖÖĆ»»·“Ó¦£¬ÓÖŅņĪŖY”¢ZÖŠŃõµÄÖŹĮæ·ÖŹż·Ö±šĪŖ50%ŗĶ40%£¬ŌņXĪŖĆ¾£¬YĪŖ¶žŃõ»ÆĮņ£¬ZĪŖŃõ»ÆĆ¾£¬WĪŖĮņ£»
£Ø2£©ČōY”¢ZĪŖĶ¬Ņ»Ö÷×å·Ē½šŹōµ„ÖŹ£¬W·Ö×Óŗ¬10øöµē×Ó£¬Ö»ÄÜŹĒSŗĶOŌŖĖŲ£»
£Ø3£©Čō¹¹³ÉXµÄŃō”¢ŅõĄė×ÓøöŹż±ČĪŖ1£ŗ2£¬ĒŅ¹¹³ÉXµÄŃō”¢ŅõĄė×ÓÖŠ·Ö±šŗ¬ÓŠ18øöŗĶ10øöµē×Ó£¬¹¹³ÉZµÄŅõ”¢ŃōĄė×ÓÖŠ¾łŗ¬ÓŠ10øöµē×Ó£¬Ōņ·ūŗĻĢõ¼žµÄ×Ŗ»ÆĪŖĒāŃõ»ÆøĘŗĶĢ¼ĖįÄĘ·“Ӧɜ³ÉNaOHŗĶĢ¼ĖįøĘ³Įµķ£»
£Ø4£©ČōX”¢Y”¢Z”¢WĖÄÖÖĪļÖŹ¾łĪŖ·Ö×Ó£¬ĒŅX·Ö×ÓÖŠŗ¬18øöµē×Ó£¬Y”¢Z·Ö×ÓÖŠ¾łŗ¬ÓŠ10øöµē×Ó£¬µ„ÖŹW·Ö×ÓÖŠŗ¬ÓŠ16øöµē×Ó£¬Ōņ·ūŗĻĢõ¼žµÄ·“Ó¦ĪŖ·śĘųŗĶĖ®µÄ·“Ó¦£®
½ā“š ½ā£ŗ£Ø1£©ČōX”¢W¾łĪŖµ„ÖŹ£¬Y”¢Z¾łĪŖŃõ»ÆĪļ£¬ÕāĖµĆ÷ĪŖÖĆ»»·“Ó¦£¬ÓÖŅņĪŖY”¢ZÖŠŃõµÄÖŹĮæ·ÖŹż·Ö±šĪŖ50%ŗĶ40%£¬ŌņXĪŖĆ¾£¬YĪŖ¶žŃõ»ÆĮņ£¬ZĪŖŃõ»ÆĆ¾£¬WĪŖĮņ£¬·“Ó¦·½³ĢŹ½ĪŖ2Mg+SO2$\frac{\underline{\;µćČ¼\;}}{\;}$2MgO+S£¬¹Ź“š°øĪŖ£ŗ2Mg+SO2$\frac{\underline{\;µćČ¼\;}}{\;}$2MgO+S£»
£Ø2£©£Ø2£©ČōY”¢ZĪŖĶ¬Ņ»Ö÷×å·Ē½šŹōµ„ÖŹ£¬W·Ö×Óŗ¬10øöµē×Ó£¬Ö»ÄÜŹĒSŗĶOŌŖĖŲ£¬¼“Įņ»ÆĒāŗĶŃõĘų²»ĶźČ«Č¼ÉÕÉś³ÉSŗĶĖ®£¬»Æѧ·½³ĢŹ½ĪŖ2H2S+O2=2S+2H2O£¬
¹Ź“š°øĪŖ£ŗ2H2S+O2=2S+2H2O£»
£Ø3£©Čō¹¹³ÉXµÄŃō”¢ŅõĄė×ÓøöŹż±ČĪŖ1£ŗ2£¬ĒŅ¹¹³ÉXµÄŃō”¢ŅõĄė×ÓÖŠ·Ö±šŗ¬ÓŠ18øöŗĶ10øöµē×Ó£¬¹¹³ÉZµÄŅõ”¢ŃōĄė×ÓÖŠ¾łŗ¬ÓŠ10øöµē×Ó£¬Ōņ·ūŗĻĢõ¼žµÄ×Ŗ»ÆĪŖĒāŃõ»ÆøĘŗĶĢ¼ĖįÄĘ·“Ӧɜ³ÉNaOHŗĶĢ¼ĖįøĘ³Įµķ£¬¼“XĪŖĒāŃõ»ÆøĘ£¬Ģ¼ĖįÄĘ£¬ZĪŖĒāŃõ»ÆÄĘ£¬WĢ¼ĖįøĘ£¬ĒāŃõ»Æøʵĵē×ÓŹ½ĪŖ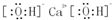 £¬
£¬
¹Ź“š°øĪŖ£ŗ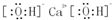 £»
£»
£Ø4£©ČōX”¢Y”¢Z”¢WĖÄÖÖĪļÖŹ¾łĪŖ·Ö×Ó£¬ĒŅX·Ö×ÓÖŠŗ¬18øöµē×Ó£¬Y”¢Z·Ö×ÓÖŠ¾łŗ¬ÓŠ10øöµē×Ó£¬µ„ÖŹW·Ö×ÓÖŠŗ¬ÓŠ16øöµē×Ó£¬Ōņ·ūŗĻĢõ¼žµÄ·“Ó¦ĪŖ2F2+2H2O=4HF+O2£¬
¹Ź“š°øĪŖ£ŗ2F2+2H2O=4HF+O2£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪļÖŹŠŌÖŹµÄ·ÖĪöÅŠ¶Ļ£¬ĪļÖŹ×Ŗ»ÆµÄĶʶĻ·½·ØŗĶĪļÖŹŠŌÖŹµÄÓ¦ÓĆ£¬ŹģÖŖø÷ÖÖ³£¼ūĪļÖŹŠŌÖŹŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®


 “ŗÓź½ĢÓżĶ¬²½×÷ĪÄĻµĮŠ“š°ø
“ŗÓź½ĢÓżĶ¬²½×÷ĪÄĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| Ļą¶Ō·Ö×ÓÖŹĮæ | ĆܶČ/£Øg•cm-3£© | ·Šµć/”ę | ČܽāŠŌ | |
| »·¼ŗ“¼ | 100 | 0.961 8 | 161 | Ī¢ČÜÓŚĖ® |
| »·¼ŗĻ© | 82 | 0.810 2 | 83 | ÄŃČÜÓŚĖ® |
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ļą¹ŲŹµŃé | Ō¤ĘŚÄæµÄ | |
| A | ŹŌŃł¼ÓĖ®Čܽāŗó£¬ŌŁ¼ÓČė×ćĮæCa£ØOH£©2ČÜŅŗ£¬ÓŠ°×É«³ĮµķÉś³É | ¼ģŃéNaHCO3¹ĢĢåÖŠŹĒ·ńŗ¬ Na2CO3 |
| B | ĻņÉŁĮæČ¼¾”»š²ńĶ·µÄ½žÅŻŅŗÖŠµĪ¼Ó×ćĮæĻ”HNO3”¢AgNO3 | ŃéÖ¤»š²ńĶ·ŗ¬ÓŠĀČŌŖĖŲ |
| C | ¼ÓČė±„ŗĶNa2CO3ČÜŅŗ£¬³ä·ÖÕńµ“£¬¾²ÖĆ”¢·Ö²ćŗ󣬷ÖŅŗ | ³żČ„ŅŅĖįŅŅõ„ÖŠµÄŅŅĖį |
| D | Į½Ö§ŹŌ¹Ü֊װӊµČĢå»ż”¢µČÅØ¶ČµÄ H2O2ČÜŅŗ£¬ĻņĘäÖŠŅ»Ö§ŹŌ¹ÜÖŠ¼ÓČė FeCl3ČÜŅŗ | Ģ½¾æFeCl3ČÜŅŗ¶ŌH2O2·Ö½āĖŁĀŹµÄÓ°Ļģ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
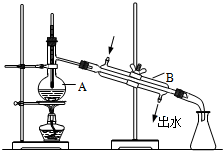 ČēĶ¼ĪŖŹµŃéŹŅÖĘČ”ÕōĮóĖ®µÄ×°ÖĆŹ¾ŅāĶ¼£¬Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£®
ČēĶ¼ĪŖŹµŃéŹŅÖĘČ”ÕōĮóĖ®µÄ×°ÖĆŹ¾ŅāĶ¼£¬Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāĀĮ»ÆŗĻĪļÓėĖ®·“Ӧɜ³ÉĒāŃõ»ÆĀĮŗĶĒāĘų | |
| B£® | ĒāĀĮ»ÆŗĻĪļÖŠĀĮĻŌ+3¼Ū£¬ĒāĻŌ-1¼Ū | |
| C£® | ĀĮÓėĖ®ÕōĘųøßĪĀĻĀ·“Ӧɜ³ÉĒāĀĮ»ÆŗĻĪļ | |
| D£® | ĒāĀĮ»ÆŗĻĪļ¾ßÓŠĒ滹ŌŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼ÓĖ®µÄĢå»żĪŖvL | |
| B£® | ¼ÓĖ®µÄÖŹĮæĪŖmg | |
| C£® | 0.5amol/LµÄ°±Ė®ÖŹĮæ·ÖŹżµČÓŚ0.5b% | |
| D£® | 0.5amol/LµÄ°±Ė®ÖŹĮæ·ÖŹżŠ”ÓŚ0.5b% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 22.4LO2Ėłŗ¬µÄ·Ö×ÓŹżÄæĪŖNA | |
| B£® | 0.5molH2Oŗ¬ÓŠµÄŌ×ÓŹżÄæĪŖ1.5NA | |
| C£® | 7.8gmolNa2O2ÓėH2O·“Ó¦×ŖŅʵē×ÓŹżÄæĪŖ0.1NA | |
| D£® | 0.5NAøöĀČĘų·Ö×ÓµÄĪļÖŹµÄĮæŹĒ0.5mol |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com