
【题目】已知:C(s)+O2(g)===CO2(g) ΔH1
CO2(g)+C(s)===2CO(g) ΔH2
2CO(g)+O2(g)===2CO2(g) ΔH3
2Cu(s)+O2(g)===2CuO(s) ΔH4
CO(g)+CuO(s)===CO2(g)+Cu(s) ΔH5
下列关于上述反应焓变的判断正确的是( )
A. ΔH1>0,ΔH3<0 B. ΔH2<0,ΔH4>0
C. ΔH2=ΔH1-ΔH3 D. ΔH3=ΔH4+ΔH1
【答案】C
【解析】
A、燃烧反应都是放热反应,ΔH1<0,ΔH3<0,ΔH4<0,反应CO2(g)+C(s)===2CO(g) 为放热反应,ΔH2>0,故A错误;B、燃烧反应都是放热反应,ΔH1<0,ΔH3<0,ΔH4<0,反应CO2(g)+C(s)===2CO(g) 为放热反应,ΔH2>0,故B错误;C、①C(s)+O2(g)===CO2(g) ΔH1;②CO2(g)+C(s)===2CO(g) ΔH2;③2CO(g)+O2(g)===2CO2(g) ΔH3;④2Cu(s)+O2(g)===2CuO(s) ΔH4;⑤CO(g)+CuO(s)===CO2(g)+Cu(s) ΔH5;由反应可知②=①-③,由盖斯定律得ΔH2=ΔH1-ΔH3,故C正确;D、由反应可知![]() ,由盖斯定律得
,由盖斯定律得![]() ,故D错误;故选C。
,故D错误;故选C。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关物质引起的。下列环境问题与所对应的物质不相关的是
A.温室效应——CO2B.白色污染——废弃塑料
C.酸雨——SO2D.雾霾——CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列化学反应的离子方程式是( )
A. 氯气溶于水:Cl2 + H2O = 2H+ + Cl-+ ClO-
B. 用碳酸钠溶液吸收少量二氧化硫:![]() =
= ![]()
C. NaClO溶液与FeCl2溶液混合:Fe2+ + 2ClO- + 2H2O = Fe(OH)2↓ + 2HClO
D. NaHSO4溶液与Ba(OH)2溶液反应至中性: H++SO42—+Ba2++OH— = BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的描述中,正确的是
A.乙醇在Cu催化下能被氧气氧化成乙醛
B.乙烯使高锰酸钾溶液和溴水褪色的原理相同
C.油脂可以水解生成氨基酸
D.葡萄糖能发生银镜反应和水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图甲、乙、丙为组成生物体的相关化合物,乙为一个由α、β、γ三条多肽链形成的蛋白质分子,共含271个氨基酸,图中每条虚线表示由两个硫基(-SH)脱氢形成一个二硫键(-S-S-)。下列相关叙述不正确的是

A. 甲为组成乙的基本单位,且乙中最多含有20种甲
B. 由不同的甲形成乙后,相对分子质量比原来少了4 832
C. 丙主要存在于细胞核中,且在乙的生物合成中具有重要作用
D. 如果甲中的R为C3H5O2,则由两分子甲形成的化合物中含有16个H
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)“高分一号”卫星使用了大功率运载火箭,火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),其反应为N2H4(l)+2H2O2(l)=N2(g)+4H2O(g),该反应生成1molH2O(g)释放出160.4kJ热量。
①H2O2的电子式为______。
②若反应后,O-H键增加了16mol,则反应释放出的热量为______kJ。
(2)镍氢蓄电池具有能量密度大、电压高、可多次反复充放电等特性,该电池放电时,正极反应式为2NiOOH+2H2O+2e-=2Ni(OH)2+2OH-,负极反应式为H2+2OH-+2e-=2H2O。
①该镍氢蓄电池放电时的电池总反应为____。
②该电池放电时,OH-向____(填“正极”或“负极”)移动。
③假设该电池放电时有2.408×1024个电子从负极流向正极,则消耗的H2在标准状况下的体积为____L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】POCl3广泛用于染料等工业。某化学学习小组借助拉瓦锡研究空气成分的曲颈甑(装置甲)合成PC13,并采取PCl3氧化法制备POCl3。
已知:(1)PCl3的熔点为-112℃,沸点为75.5℃,遇水生成H3PO3和HCl;
(2)2PCl3+O2==2POCl3。
【实验Ⅰ】制备PCl3
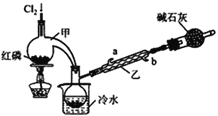
(1)实验室制备Cl2的原理是________________________。
(2)碱石灰的作用除了处理尾气外还有________________________。
(3)装置乙中冷凝水从_____(选填a或b)进入。
【实验Ⅱ】制备POCl3
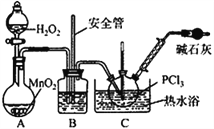
(4)实验室常用有微孔的试剂瓶保存H2O2,“微孔”与上述装置中的___________(仪器名称)目的是一致的。
(5)C中反应温度控制在60~65℃,其原因是________________________。
【实验Ⅲ】测定POCl3含量
①准确称取30.70gPOC13产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解;
②将水解液配成100.00mL溶液,取10.00mL溶液于锥形瓶中;
③加入10.00mL3.200mol/LAgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;
④以Fe3+ 为指示剂,用0.2000mol/LKSCN 溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00 mL KSCN 溶液。
已知:Ag++SCN-==AgSCN↓ Ksp(AgCl)>Ksp(AgSCN )。
(6)POC13水解的化学反应方程式为________________________。
(7)滴定终点的现象为____________,用硝基苯覆盖沉淀的目的是________________________。
(8)反应中POC13的百分含量为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法中,不正确的是
A.硅可用作半导体材料
B.氯气可用于制取漂白粉
C.二氧化硅可用于制造光导纤维
D.浓硫酸可以干燥NH3、H2等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了A~X元素在周期表中的位置,填写下列空白:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
一 | A | |||||||
二 | L | M | Q | |||||
三 | D | G | J | R | X | |||
四 | E | T |
(1)这些元素中,化学性质最不活泼的是:______(用具体元素符号或化学式等化学用语填空,下同)。
(2)在最高价氧化物对应的水化物中,酸性最强的化合物是________,该化合物与性质表现为两性氢氧化物的物质反应的离子方程式为__________________________________。
(3)G元素与T元素形成的化合物属于_______(填“共价”或“离子”)化合物。
(4)D、E、G三种元素按原子半径由大到小的顺序排列__________________。
(5)A元素的单质分别与M元素的单质、R元素的单质反应生成甲、乙,甲、乙常温下均为气态,且两者相遇时可化合成丙。化合物丙的电子式为_____________。
(6)R元素和T元素两者核电荷数之差是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com