
| A、MnO2+4HCl=MnCl2+2H2O+Cl2↑ | ||||
| B、2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O | ||||
| C、5Cl2+I2+6H2O=10HCl+2HIO3 | ||||
D、2NaCl+2H2O
|
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A、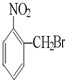 |
B、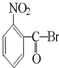 |
C、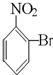 |
D、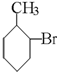 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下;22.4LH2O中共价键数目为2NA |
| B、12g金刚石的σ键数目为4 NA |
| C、16gO2与O3的混合气体中氧原子数目为NA |
| D、标准状况下1.12L乙炔中π键数目为0.05 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.9%氯化钠溶液 |
| B、0.9%氯化铵溶液 |
| C、1.25%碳酸氢钠溶液 |
| D、5%葡萄糖溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子式为C8H10且属于芳香烃的同分异构体有4种 |
| B、C3H8光照下与氯气反应,最多能生成四种二氯代烃 |
| C、戊烷有3种同分异构体 |
| D、甲苯苯环上的一个氢原子被丙基取代,所得产物有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、E元素处于元素周期表中第3周期第ⅦA族 |
| B、元素A、B、C的原子半径:C>B>A |
| C、元素B、C、D的非金属性:C>B>D |
| D、一定条件下,A单质可以将D单质从其氧化物中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、+184.6kJ?mol-1 |
| B、+92.3kJ?mol-1 |
| C、-184.6kJ?mol-1 |
| D、-92.3kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如下表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如下表:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
| ① |
| ② |
| ③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com