
海带中含碘元素,从海带中提取碘有如下步骤:①通入足量Cl2;②将海带焙烧成灰后加水搅 拌;③加CCl4振荡;④用分液漏斗分液;⑤过滤。则合理的操作顺序是
A.①②③④⑤ B.②⑤①③④
C.①③⑤②④ D.②①③⑤④
科目:高中化学 来源:2014-2015学年河北省高一12月月考化学试卷(解析版) 题型:填空题
(10分)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下
3Cu + 8HNO3 == 3Cu(NO3)2 + 2NO↑+ 4H2O
(1)上述反应中氧化剂与氧化产物的物质的量之比 。
(2)若生成NO的体积为3.36L(标准状况),且硝酸足量,则消耗铜的质量 g,转移电子的数目为 ,被还原的硝酸为 mol。
(3)写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二12月月考化学试卷(解析版) 题型:选择题
下列溶液一定呈中性的是
A.c(H+)=c(OH-)=10-6 mol·L-1的溶液
B.pH=7的溶液
C.使石蕊试液呈紫色的溶液
D.酸与碱恰好完全反应生成正盐的溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高一上学期第三次月考化学试卷(解析版) 题型:填空题
(14分)铝是应用最广泛的金属之一,铝的化合物在生产和生活中也有许多用途。
(1)铝在反应中容易失去电子,发生 反应(填氧化或还原),生成铝离子,铝离子的结构示意图是 。
(2)生产中曾用铝热反应焊接钢轨,写出铝与氧化铁发生反应的化学方程式为并标出电子转移的方向和数目: 。
(3)胃舒平是治疗胃酸过多的常用药物,其中含有的有效成分是氢氧化铝,其治疗原理是(用离子方程式表示): ;
(4)在同温同压下,等质量的铝分别投入足量的稀盐酸和NaOH溶液中,产生气体的体积之比为 。
(5)铝合金在空气中很稳定,可以制造多种建筑型材。向一只小烧杯里加入少量CuSO4溶液,把一小块铝合金浸入溶液中,1~2分钟后将铝合金取出,无明显现象。将另一小块铝合金先放入NaOH溶液里,片刻后取出,用蒸馏水冲洗后浸入CuSO4溶液里,1~2分钟后将铝片取出,发现铝片表面有亮红色的固体附着,NaOH溶液的作用是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.二氧化硫溶于水能导电,故二氧化硫属于电解质
B.硫酸钡难溶于水,故硫酸钡属于弱电解质
C.硫酸是强电解质,故纯硫酸能导电
D.氢离子浓度相同的盐酸和醋酸溶液导电能力相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高二上学期第三次月考化学试卷(解析版) 题型:填空题
(16分)碳及其化合物应用广泛。
I 工业上利用CO和水蒸汽反应制氢气,存在以下平衡:
CO(g)+H2O(g)  CO2(g)+H2(g) △H>0
CO2(g)+H2(g) △H>0
(1)向1L恒容密闭容器中注入CO(g)和H2O(g),830℃时测得部分数据如下表。则该温度下反应的平衡常数K=______________。
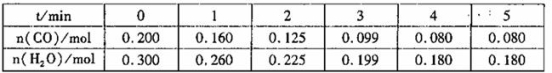
(2)相同条件下,向1L恒容密闭容器中,同时注入2mol CO、2mol H2O(g),1molCO2和1mo1H2,此时v(正 ) __________v(逆)(填“>”“=”或“<”)
(3)上述反应达到平衡时,要提高CO的转化率,可采取的措施是_______(填字母代号)。
A.升高温度
B.加入催化剂
C.增大压强
D.增加CO的浓度
E.及时分离出CO2
II 已知CO(g)+1/2 O2 (g)=CO2 (g) △H=一141 kJ·mol-1
2H2(g)+ O2(g)=2H2O(g) △H=一484 kJ·mol-1
CH3OH(1)+3/2O2 (g)=CO2(g)+2H2O(g) △H=一726 kJ·mol-1
(4)用CO(g)、H2(g)化合制得液态甲醇的热化学方程式为___________________________。
III某同学设计了一个甲醇燃料电池,并用该电池电解100mL一定浓度NaCl与CuSO4混合溶液,其装置如图:

(5)写出甲中通入甲醇这一极的电极反应式__________________________________ 。
(6)理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式____________,原混合溶液中CuSO4的物质的量浓度____________mol/L。(假设溶液体积不变)
(7)将在t2时所得的溶液稀释至200mL,该溶液的pH约为___________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高二上学期第三次月考化学试卷(解析版) 题型:选择题
往2L密闭容器中充入NO2,在三种不同条件下发生反应:
实验测得NO2的浓度随时间的变化如下表(不考虑生成N2O4)。

下列说法正确的是
A.实验2比实验1的反应容器体积减小
B.实验2比实验l使用了效率更高的催化剂
C.实验2和实验3可判断该反应是放热反应
D.实验1比实验3的平衡常数大
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省等四校高一上学期期中联考化学试卷(解析版) 题型:填空题
(6分)在下列物质中选择溶于水后可以电离的物质,并写出相应的电离方程式(有几个写几个):①硝酸铵(NH4NO3) ②葡萄糖[C6H12O6] ③氢氧化钡[Ba(OH)2] ④硫酸(H2SO4) ⑤四氯化碳(CCl4)
。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海理工大学附中高三上学期月考化学试卷(解析版) 题型:选择题
物质制备过程中离不开物质的提纯。以下除杂方法不正确的是
选项 | 目的 | 实验方法 |
A | 除去Na2CO3固体中的NaHCO3 | 置于坩埚中加热至恒重 |
B | 除去NaCl中少量KNO3 | 将混合物制成热饱和溶液,冷却结晶,过滤 |
C | 除去CO2中的HCl气体 | 通过NaHCO3(aq,饱和),然后干燥 |
D | 除去C2H5Br中的Br2 | 加入足量Na2SO3(aq),充分振荡,分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com