
| A. | 仅①② | B. | 仅①②③ | C. | 仅①②③④ | D. | 全部 |
分析 ①根据可燃性气体遇明火可能发生爆炸进行解答;
②由于浓硫酸的密度比水大,且易溶于水,溶于水时放出大量的热,所以稀释时一定要把浓硫酸慢慢倒入水中;
③根据碱液的腐蚀性分析;
④根据给液体加热注意事项进行解答;
⑤根据酒精灯的正确使用方法去分析.
解答 解:①可燃性气体遇明火可能发生爆炸,所以在点燃H2、CO、CH4等易燃气体前.必须检验气体的纯度,故①正确;
②稀释浓硫酸时,要考虑浓硫酸的物理性质,密度比水大,易溶于水,溶于水时放出大量的热,如果把水倒入浓硫酸中,水会浮在上面,放出的热足以使水沸腾,从而造成液滴飞溅,导致事故发生,所以稀释浓硫酸时要把浓硫酸倒入水中,并不断搅拌,使热量快速扩撒,故②正确;
③浓碱对皮肤有腐蚀性,如不慎溅到皮肤上,应用较多的水冲洗,然后再涂上硼酸溶液,故③正确;
④给液体加热注意事项:给试管中的液体加热,液体一般不超过试管容积的$\frac{1}{3}$,故④正确;
⑤向酒精灯内添加酒精时一般不超过酒精灯容积的三分之二,不少于酒精灯容积的三分之一,点燃添满酒精的酒精灯易发生事故,故⑤错误;故选C.
点评 本题考查实验安全及操作,注意化学实验要严格遵守操作规程,题目难度不大,旨在考查学生的基础知识的掌握,化学实验是化学的基础,要了解常见的实验操作,能对错误操作的后果做出判断,养成良好的实验习惯.


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案科目:高中化学 来源: 题型:多选题
| A. | 1:3 | B. | 2:3 | C. | 1:4 | D. | 2:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度相等、体积相同的O2和N2 | B. | 质量相等、密度不等的N2和C2H4 | ||
| C. | 体积相等、密度相等的CO和O2 | D. | 压强相等、体积相同的N2O和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:1:2:1 | B. | 1:3:2:2 | C. | 1:3:1:2 | D. | 3:1:2:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 三种金属的物质的量相等 | |
| B. | 三种金属可能均过量 | |
| C. | 三种金属的质量相等 | |
| D. | 参加反应的三种金属的质量比为12:9:28 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三聚氰胺的摩尔质量为126 | |
| B. | 用三聚氰胺制造的餐具不可以放进微波炉中加热使用 | |
| C. | 三聚氰胺中C、N两种元素的质量比为3:7 | |
| D. | 三聚氰胺中氮元素的质量分数约为66.7% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 6种 | C. | 9 种 | D. | 12种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①③⑥ | C. | ②④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
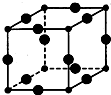 Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用.
Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用.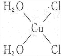 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com