
【题目】用“KClO3氧化法”制备KIO3的工艺流程如下图所示,其中“酸化反应”所得到的产物有KH(IO3)2、Cl2和KCl。下列叙述错误的是
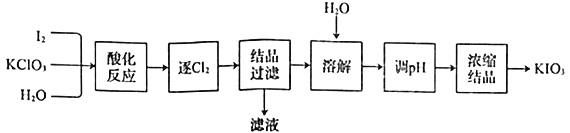
A.KIO3可作为食盐中的补碘剂
B.“逐Cl2”采用的方法通常是加热
C.“滤液”中的溶质主要是KCl
D.“调pH”步骤中所加入的试剂是NaOH
科目:高中化学 来源: 题型:
【题目】将3.48gFe3O4完全溶解在100mL 1mol·L-1H2SO4溶液中,然后加入K2Cr2O7溶液25mL,恰好使溶液中的Fe2+全部反应完,Cr2O72-全部转化为Cr3+,则K2Cr2O7溶液的物质的量浓度为
A.0.033mol·L—1B.0.3mol·L—1C.0.2mol·L—1D.0.1mol·L—1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,6己二酸(G)是合成高分子化合物尼龙的主要原料之一,可用烃A氧化制备。制备G的合成路线如下:
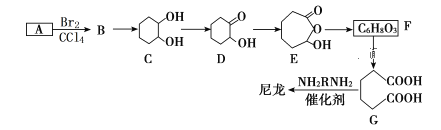
(1)A的化学名称为__________________。C→D的反应类型为_______________。
(2)D中官能团的名称________________。E的分子式为_________________。
(3)F的结构简式为___________________。
(4)写出B→C的化学反应方程式_________________________________________。
(5)写出能同时满足下列条件的G的同分异构体的结构简式_________________。
①与G具有相同的官能团
②核磁共振氢谱中有三组峰,面积比为3∶1∶1
(6)由A通过两步反应制备1,3环己二烯的合成路线____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M(![]() )、N(
)、N(![]() )、P(
)、P(![]() )都是重要的有机物。下列有关M、N、P的说法正确的是( )
)都是重要的有机物。下列有关M、N、P的说法正确的是( )
A.M与HBr发生加成反应的产物只有一种
B.P中所有碳原子一定共平面
C.M、N、P互为同分异构体
D.M能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有CO、NOx等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
(1)已知 4CO(g)+2NO2(g)![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol1
①该反应在________________(填“高温、低温或任何温度”)下能自发进行。
②对于该反应,改变某一反应条件(温度T1>T2),下列图象正确的是_______(填序号)。
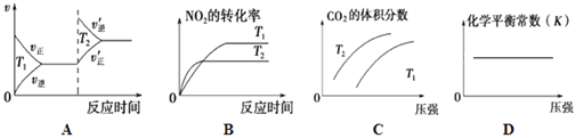
③某实验小组模拟上述净化过程,一定温度下,在2L的恒容密闭容器中,起始时按照甲、乙两种方式进行投料,经过一段时间后达到平衡状态,测得甲中CO的转化率为50%,则该反应的平衡常数为__________;两种方式达平衡时,N2的体积分数:甲______乙( 填“>、=、<或不确定”,下同),NO2的浓度:甲______乙。

(2)柴油汽车尾气中的碳烟(C)和NOx可通过某含钴催化剂催化消除。不同温度下,将模拟尾气(成分如下表所示)以相同的流速通过该催化剂测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图所示。
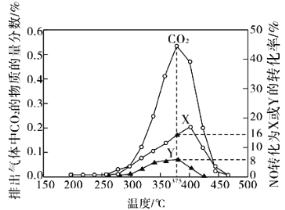
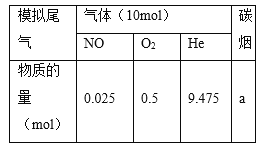
①375℃时,测得排出的气体中含0.45 mol O2和0.0525 mol CO2,则Y的化学式为________。
②实验过程中采用NO模拟NOx,而不采用NO2的原因是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种光化学电池的结构如图所示,电池总反应为AgCl(s)+ Cu+(aq) = Ag(s)+Cu2+(aq)+Cl-(aq),下列关于该电池在工作时的说法中不正确的是
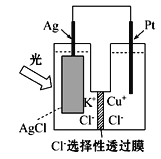
A.电子的运动方向:Pt→外电路→Ag→内电路→PtB.生成108 g银,转移的电子为1 mol
C.Cu+在负极发生氧化反应D.Cl-由正极迁移到负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌及锌的化合物应用广泛。例如,测定铜合金中的铅、锌时要利用锌配离子的下列反应:[Zn(CN)4]2-+4HCHO+4H2O=Zn2++4HOCH2CN+4OH-
回答下列问题:
(1)基态Zn2+的电子排布式为_____________,基态 C原子核外电子占据_____个不同原子轨道。
(2)C、N、O三种元素的第一电离能由大到小的顺序为___________,HOCH2CN分子中含有的σ键与π键数目之比为_________。
(3)HCHO分子中碳原子轨道的杂化类型是________,福尔马林是HCHO的水溶液,HCHO极易与水互溶的主要原因是_________________________。
(4)[Zn(CN)4]2-中Zn2+与CN-之间的化学键称为_________,提供孤电子对的成键原子是________。
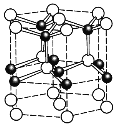
(5)ZnO的一种最稳定的晶体结构如图所示,晶胞中Zn2+的配位数为______。六棱柱底边长为acm,高为bcm,设阿伏加德罗常数的值为NA,则ZnO的密度为_______ g/cm3(列出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. ![]() 的溶液中:K+、Na+、CO32-、NO3-
的溶液中:K+、Na+、CO32-、NO3-
B.澄清透明的溶液中:Fe3+、Mg2+、SCN-、Cl-
C.c(Fe2+)=1 mol/L的溶液中: Na+、NH4+、AlO2-、SO42-
D.能使甲基橙变红的溶液中: K+、NH4+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早在1774年,瑞典化学家舍勒在研究软锰矿(主要成分![]() )的过程中,将它与浓盐酸混合加热,产生了黄绿色气体—氯气。某小组同学利用舍勒发现氯气的方法制取氯气并探究其性质。
)的过程中,将它与浓盐酸混合加热,产生了黄绿色气体—氯气。某小组同学利用舍勒发现氯气的方法制取氯气并探究其性质。

请回答:
(1)装置①中制取氯气,盛有浓盐酸的玻璃仪器名称为__________
(2)装置②的作用是________________________________________.
(3)装置③中的现象是________________________________________.
(4)装置④中反应的离子方程式是________________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com