
| A. | FeCl3 NaOH KCl | B. | KCl Na2CO3 Na2SO4 | ||
| C. | BaCl2 NaCl Na2SO4 | D. | NaCl AgNO3 KCl |
科目:高中化学 来源: 题型:选择题
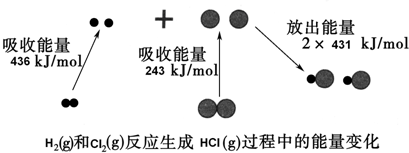
| A. | 1 mol H2(g)和1 mol Cl2(g)具有的总能量大于2 mol HCl(g)具有的总能量 | |
| B. | 该反应的△H>0 | |
| C. | 通常情况下,H2(g)和Cl2(g)混合容易直接生成HCl(g) | |
| D. | 生成的HCl溶于水会发生电离,即HCl=H++Cl-,由此判断,HCl中存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于0.3mol | B. | 大于0.3mol | ||
| C. | 大于0.3mol,小于0.6mol | D. | 等于0.6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜和稀硫酸反应:Cu+2H+=Cu2++H2↑ | |
| B. | NaHCO3溶液与HCl溶液反应:H++HCO3-=CO2↑+H2O | |
| C. | 铝和硫酸铜溶液的反应Al+Cu2+=Al3++Cu | |
| D. | 氯化铁滴入沸水中生成氢氧化铁胶体Fe3++3H2O=Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②④ | C. | ①③ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D>C>A>B | B. | D>A>B>C | C. | D>B>A>C | D. | B>A>D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量浓度相同 | B. | 氢氧根离子浓度相同 | ||
| C. | pH相同 | D. | 溶液中离子浓度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com