
| A. | Fe2(SO4)3溶液在空气中加热蒸干并灼烧后,可以得到Fe2(SO4)3 | |
| B. | 为除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下,加入氨水,过滤后向滤液中再加入适量盐酸 | |
| C. | 配制FeSO4溶液时,为了抑制亚铁离子水解,需加入少量Fe | |
| D. | 室温下,向PH=4的醋酸溶液中加入等体积的PH=10的NaOH溶液,反应后溶液呈碱性,是因为生成了强碱弱酸盐 |
分析 A.硫酸铁水解生成氢氧化铁和硫酸,当溶液蒸干时,得到的固体是硫酸铁;
B.除杂需要加入试剂调节溶液PH使铁离子沉淀,但不能引入新的杂质;
C.FeSO4溶液易被氧化为硫酸铁,加入铁可以防止Fe2+被氧化;
D.醋酸溶液中存在电离平衡,隋风云进行醋酸又电离出氢离子.
解答 解:A.硫酸铁水解生成氢氧化铁和硫酸,加热促进硫酸铁水解,因为硫酸没有挥发性,所以得到的固体仍然是Fe2(SO4)3,硫酸铁水解离子方程式为Fe3++3H2O?Fe(OH)3+3H+,故A正确;
B.加入氨水混入氯化铵杂质,且生成氢氧化镁沉淀,故B错误;
C.FeSO4溶液易被氧化为硫酸铁,加入铁可以防止Fe2+被氧化,不是抑制水解,故C错误;
D.室温下,向PH=4的醋酸溶液中加入等体积的PH=10的NaOH溶液,反应后促进醋酸电离,溶液呈酸性,故D错误;
故选A.
点评 本题考查了盐类水解、除杂方法、酸碱反应后溶液酸碱性判断,注意弱电解质电离平衡的分析,掌握基础是解题关键,题目难度中等.


 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:实验题
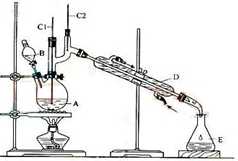 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.72 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使 SO3 的浓度增大 | B. | 使平衡向正反应方向移动 | ||
| C. | 使平衡常数 K 增大 | D. | 使正反应速率大于逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x:y=3:1 | B. | v(A):v(C)=2:1 | ||
| C. | A的平衡浓度为0.4mol/L | D. | A与B的平衡浓度之比为3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L 水蒸气含有的分子数为1NA | |
| B. | 常温常压下,32 g O2含有的原子数为2个 | |
| C. | 常温常压下,NA个CO2分子占有的体积为22.4 L | |
| D. | 体积为1L、物质的量浓度为0.5 mol/L的氯化钙溶液中,含有Cl-个数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com