
某无色透明酸性溶液中,能大量共存的离子组是
A.Na+、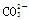 、Cu2+、
、Cu2+、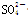 B.K+、Fe3+、
B.K+、Fe3+、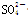 、OH-
、OH-
C.Ca2+、NO3-、Cl-、K+ D.Ba2+、K+、MnO4_、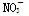
 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源:2014-2015学年宁夏育才中学高二上学期期中化学试卷(解析版) 题型:实验题
(4分)在25℃时,有pH为a的HCl溶液和pH为b的NaOH溶液,取VaL该盐酸溶液用该NaOH溶液中和,需VbL NaOH溶液,(题中a≤b,b≥8)。问:
(1)若a+b=14,则Va/Vb= .
(2)若a+b=13,则Va/Vb=
(3)若a+b>14,则Va/Vb= ,且Va Vb(填“>”“<”“=”)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列各组微粒的空间构型相同的是
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和C2H2 ⑥SiO44-和SO42-
A.全部 B.除①④⑥以外 C.③④⑤⑥ D.②⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏回族自治区银川一中高一上期中化学试卷(解析版) 题型:填空题
现有以下物质:
①NaCl固体 ②盐酸 ③Ba(OH)2溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体
⑦乙醇(C2H5OH) ⑧液态硫酸 ⑨熔融态BaSO4 ⑩液态SO3
请回答下列问题(用序号):
以上物质中属于化合物的是 (填序号,下同),属于盐的是 ,属于氧化物的是 ,能导电的是_______________________,属于电解质的是______________________,属于非电解质的是___________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏回族自治区银川一中高一上期中化学试卷(解析版) 题型:选择题
能正确表示下列化学反应的离子方程式的是
A.碳酸钠溶于足量盐酸中 Na2CO3+2H+=2Na++CO2?+H2O
B.氧化钠与稀硫酸的反应 Na2O+2H+ = 2Na++H2O
C.氢氧化钡溶液与硫酸铜溶液反应 Ba2+ + 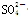 = BaSO4↓
= BaSO4↓
D.铁片插入稀硫酸溶液中 Fe + 2H+ = Fe3+ + H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏回族自治区银川一中高一上期中化学试卷(解析版) 题型:选择题
在相同的温度和压强下,二氧化氮和二氧化碳两种气体的分子数相同,则下列它们的( )一定相同。
(1)体积 (2)所含原子个数 (3)物质的量 (4)质量 (5)密度
A.只有(1)(2)(3) B.只有(1)(2)(4)
C.只有(2)(3)(5) D.(1)(2)(3)(4)(5)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏回族自治区银川一中高一上期中化学试卷(解析版) 题型:选择题
下列对于“摩尔”的说法和理解正确的是
A.摩尔是国际科学界建议采用的一种物理量
B.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
C.国际上规定,0.012kg碳原子所含有的碳原子数目为1摩
D.摩尔是物质的量的单位,简称摩,符号为mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏回族自治区银川一中高二上学期期中化学试卷(解析版) 题型:选择题
在同温同压下,下列各组热化学方程式中,△H2>△H1的是
A.2H2(g)+O2(g)=2H2O(g) △H1;2H2(g)+O2(g)=2H2O(l) △H2
B.S(g)+O2(g)=SO2(g)△H1;S(s)+O2(g)=SO2(g) △H2
C.C(s)+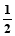 O2(g)=CO(g)△H1;C(s)+O2(g)=CO2(g) △H2
O2(g)=CO(g)△H1;C(s)+O2(g)=CO2(g) △H2
D.H2(g)+Cl2(g)=2HCl(g)△H1;2H2(g)+2Cl2(g)=4HCl(g) △H2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高二上学期期中化学试卷(解析版) 题型:填空题
(10分)硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为: H2SO4=H++HSO4-,HSO4- H++SO42-。.
H++SO42-。.
请据此回答下列有关问题:
(1)Na2SO4溶液呈 (填“弱酸性”、“中性”或“弱碱性”),原因是: (用离子方程式表示)。
(2)写出H2SO4溶液与BaCl2溶液反应的离子方程式: ;
(3)在0.1 mol·L-1的Na2SO4溶液中,下列粒子浓度关系式正确的是 。(填编号)
A.c(SO42-)+c(HSO4-)=0.1 mol·L-1
B.c(SO42-)+c(HSO4-)=2c(Na+)
C.c(OH-)=c(H+)+c(HSO4-)
D.c(Na+)+c(H+)=c(OH-)+c(HSO4-)
(4)已知0.1 mol·L-1的NaHSO4溶液的pH=2,则0.1 mol·L-1的H2SO4溶液中SO42-的浓度 0.01mol·L-1(填“>”“=”或“<”),原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com